Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

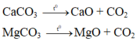
Gọi số mol C a C O 3 và M g C O 3 lần lượt là a và b mol
→ 100a + 84b = 30 (gam) (1)
Theo bài ra khối lượng chất rắn sau phản ứng là 30 : 2 = 15 gam
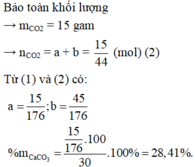
⇒ Chọn A.

Gọi số mol FeCO3, ZnCO3 là a, b (mol)
PTHH: FeCO3 --to--> FeO + CO2
a----------->a
ZnCO3 --to--> ZnO + CO2
b--------->b
mbđ = 116a + 125b (g)
msau pư = 72a + 81b (g)
=> \(\dfrac{72a+81b}{116a+125b}=\dfrac{6,21}{9,73}\)
=> 19,8a = 11,88b
=> a = 0,6b
\(\%m_{FeCO_3}=\dfrac{116a}{116a+125b}.100\%=\dfrac{116.0,6b}{116.0,6b+125b}.100\%=35,766\%\)
=> \(\%m_{ZnCO_3}=100\%-35,766\%=64,234\%\)
Với các bài tập chỉ có tỉ lệ và phần trăm, có thể đặt một lượng chất bất kì. Đối với bài này, đặt khối lượng chất rắn thu được là 6,21 gam, khối lượng muối ban đầu là 9,73 gam
FeCO3 → FeO + CO2 ZnCO3 → ZnO + CO2
a a b b mol
mFeCO3 + mZnCO3 = 116a + 125b = 9,73 gam
mFeO + mZnO = 72 + 81b = 6,21 gam
a = 0,03 mol; b = 0,05 mol

Gọi khối lượng hỗn hợp ban đầu là 100 g , số mol MgCO3 và CaCO3 lẫn lượt là x và y.
Ta có : 84x+ 100y=100 (g) (1)
PTHH: MgCO3 –to-> MgO + CO2
CaCO3 –to-> CaO + CO2
-> Khối lượng giảm là CO2
-> số mol CO2 là : x+y= 47,5 : 44= 1,08(mol) (2)
Từ (1) và (2) ta suy ra:
x= 0,5(mol)
y= 0,58( mol)
=> % MgCO3 =42%
% CaCO3 = 58%.
Gọi khối lượng hỗn hợp ban đầu là 100 g , số mol MgCO3 và CaCO3 lẫn lượt là x và y.
Ta có : 84x+ 100y=100 (g) (1)
PTHH: MgCO3 ➞ MgO + CO2
CaCO3 ➞ CaO + CO2
-> Khối lượng giảm là CO2
-> số mol CO2 là : x+y= 47,5 : 44= 1,08(mol) (2)
Từ (1) và (2) ta suy ra:
x= 0,5(mol)
y= 0,58( mol)
=> % mMgCO3 =42%
%mCaCO3 = 58%.

a. Các phương trình có thể xảy ra:
C + O2 → t ∘ CO2 (1)
CaCO3 → t ∘ CaO + CO2 (2)
MgCO3 → t ∘ MgO + CO2 (3)
CuCO3 → t ∘ CuO + CO2 (4)
C +CO2 → t ∘ 2CO (5)
C + 2CuO → t ∘ 2Cu + CO2 (6)
CO + CuO → t ∘ Cu + CO2 (7)
CaO + 2HCl →CaCl2 + H2O (8)
MgO + 2HCl →MgCl2 + H2O (9)
CuO + 2HCl →CuCl2 + H2O (10)
b. Vì sau phản ứng có CO và CO2, các phản ứng xảy ra hoàn toàn nên các chất còn lại sau khi nung là CaO, MgO và Cu không có phản ứng (10)
mCu = 3,2(g) => mCuCO3 = 6,2g
Gọi số mol CaCO3, MgCO3, C trong hỗn hợp lần lượt là a, b, c.(*)
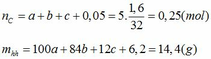
Giải ( *), (**), (***) ta được a=0,025; b=0,05; c=0,125.
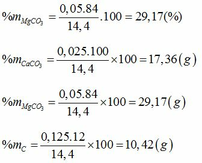

PTHH:
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
0,15 0,15
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Ta có: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,15\cdot100=15\left(g\right)\)
\(\Rightarrow m_{CaO}=20,6-15=5,6\left(g\right)\)
\(\Rightarrow\%m_{CaCO_3}=\dfrac{15\cdot100}{20,6}\approx73\%\)
\(\Rightarrow\%m_{CaO}=100\%-73\%=27\%\)

MgCO3---->MgO+CO2
x--------------------x--x
CaCO3------->CaO+CO2
y------------------y---------y
n CO2=1,68/22,4=0,075(mol)
Theo bài ra ta có hpt
\(\left\{{}\begin{matrix}40x+56y=3,8\\x+y=0,075\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,025\\y=0,05\end{matrix}\right.\)
m hh=3,8+0,075.44=7,1(g)
%m MgCO3=0,025.84/7,1.100%=29,58%
%m CaCO3=100%-29,58=70,42%
Chúc bạn học tốt

Gọi số mol MgCO3, CaCO3 là a, b (mol)
=> 84a + 100b = 1,84 (1)
PTHH: MgCO3 --to--> MgO + CO2
a-------------------->a
CaCO3 --to--> CaO + CO2
b-------------------->b
=> a + b = \(\dfrac{0,448}{22,4}=0,02\) (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,01.84}{1,84}.100\%=45,65\%\\\%m_{CaCO_3}=\dfrac{0,01.100}{1,84}.100\%=54,35\%\end{matrix}\right.\)

Giả sử hỗn hợp ban đầu có khối lượng là 100g
CaCO3 ---to ----> CaO + CO2
Khối lượng sau =78% khối lượng hỗn hợp ban đầu
=> \(m_{sau}=100.78\%=78\left(g\right)\)
=> \(m_{giảm}=m_{CO_2}=22\left(g\right)\)
=> \(n_{CO_2}=0,5\left(mol\right)\)
Ta có : \(n_{CaCO_3}=n_{CO_2}=0,5\left(mol\right)\)
=> \(\%m_{CaCO_3}=\dfrac{0,5.100}{100}.100=50\%\)
=> %mNaCl = 50%
gọi số mol CaCO3 là x, số mol MgCO3 là y
CaCO3 -> CaO + CO2\(\uparrow\)
x -> x -> x
MgCO3 -> MgO + CO2\(\uparrow\)
y -> y -> y
ta có pt:
56x + 40y = (100x + 84y)/2
<=> 112x + 80y = 100x + 84y
<=> 12x = 4y
<=> 3x = y
=> % CaCO3 là 100/4 * 3 = 75%
% MgCO3 là 25%