Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
2Fe(OH)3 → t o Fe2O3 + 3H2O
4Fe(OH)2 + O2 → t o 2Fe2O3 + 4H2O
FeO, Fe3O4 + O2 → Fe2O3
Fe(NO3)2, Fe(NO3)3 → Fe2O3
=> chất rắn A. Fe2O3
Chú ý:
nhiệt phân trong không khí =>Các oxit sắt chuyển hết thành Fe2O3

Khi nung hỗn hợp các chất F e N O 3 2 , F e ( O H ) 3 v à F e C O 3 trong không khí đến khối lượng không đổi, thu được một chất rắn là F e 2 O 3 .
Chọn đáp án D.

Đáp án B
nHNO3 = 0,72 mol ; nNaOH = 0,3 mol ; nKOH = 0,15 mol
Đặt nFe = x ; nCu = y => nFe2O3 = 0,5x ; nCuO = y
Ta có : 56x + 64y = 11,1g ; 80x + 80y = 15
=> x = 0,1125 ; y = 0,075
Giả sử chất rắn khan sau khi nung T gồm 0,3 mol NaNO2 và 0,15 mol KNO2
mT = 0,3.69 + 0,15.85 = 33,45g > 322,145g => trong chất rắn khan sau nung T có cả bazo dư
Đặt nNO2 = a ; nOH = b
0,3.23 + 0,15.39 + 46a + 17b = 32,145
a + b = 0,45
=> a = 0,405 ; b = 0,045
Do nNO3 muối = 0,405 < 3nFe + 2nCu = 3.0,1125 + 2.0,075 = 0,4875
=> Sản phẩm có cả Fe2+ và Fe3+ và HNO3 phản ứng hết.
Trong dung dịch X có : z mol Fe2+ ; t mol Fe3+ ; 0,075 mol Cu2+ ; 0,405 mol NO3-
Bảo toàn Fe : z + t = 0,1125
Bảo toàn điện tích : 2z + 3t + 2.0,075 = 0,405
=> z = 0,0825 và t = 0,03
Bảo toàn H : nH2O = ½ nHNO3 = 0,36 mol
Bảo toàn khối lượng : msp khử = mHNO3 – mNO3 muối – mNO3 (X) – mH2O = 13,77g
mdd X = mKL + mdd HNO3 – msp khử = 91,83g
=> C% Fe(NO3)3 = 7,91%

Đáp án B
Giả sử KOH không dư ⇒ nKNO2 = nKOH = 0,5 mol ⇒ mrắn ≥ mKNO2 = 42,5(g)
⇒ vô lí! ⇒ KOH dư. Đặt nKNO3 = x; nKOH dư = y. Bảo toàn nguyên tố Kali: x + y = 0,5.
Rắn gồm KNO2 và KOH dư ⇒ 85x + 56y = 41,05 ⇒ giải hệ có: x = 0,45 mol; y = 0,05 mol.
Đặt nFe = a; nCu = b ⇒ mA = 56a + 64b = 11,6(g)
16(g) rắn gồm Fe2O3 và CuO.
⇒ 160.0,5a + 80b = 16
⇒ giải hệ có: a = 0,15 mol; b = 0,05 mol.
nHNO3 = 0,7 mol; nNO3–/X = nKNO3 = 0,45 mol. Bảo toàn nguyên tố Nitơ: nN/B = 0,25 mol.
Bảo toàn nguyên tố Hidro: nH2O = 0,35 mol. Bảo toàn nguyên tố Oxi: nO/B = 0,4 mol.
⇒ Bảo toàn khối lượng: mX = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2(g).
-> nNO3–/X < 3nFe + 2nCu ⇒ X gồm muối Fe(NO3)2, Fe(NO3)3 và Cu(NO3)2.
Giải hệ có: nFe(NO3)3 = 0,05 mol
⇒ C%Fe(NO3)3 = 0,05 × 242 ÷ 89,2 × 100% = 13,56%
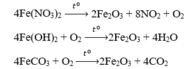
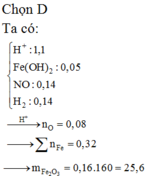
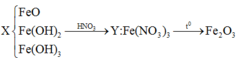

Chọn đáp án D
Chú ý: Fe(NO3)2 và FeCO3 nung sẽ thu được Fe2O3 chứ không phải FeO
=> HS tránh nhầm lẫn sẽ Chọn đáp án B