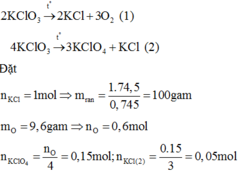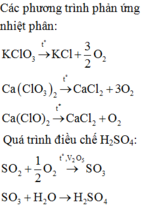Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

KClO3 vừa có tính oxi hóa vừa có tính khử
(1) KClO3 (O-2 → O0)
(2) KClO3 (O+5 → O+7)

Gọi x là số mol KCl O 3 bị phân huỷ theo (a).
Gọi y là số mol KCl O 3 bị phân huỷ theo (b).
2KCl O 3 → 2KCl + 3 O 2
4KCl O 3 → 3KCl O 4 + KCl
Ta có x + y = 73,5/122,5 = 0,6 (1)
x + y/4 = 33,5/74,5 = 0,45 (2)
Từ (1) và (2) , giải ra:
x =0,4 → phần trăm KCl O 3 bị phân hủy theo (a) là: 0,4/0,6 x 100 % = 66,66%
y =0,2 → phần trăm KCl O 3 bị phân hủy theo (b) là: 0,2/0,6 x 100 % = 33,34%

Đáp án C
MnO2 là chất xúc tác nên sử dụng định luật bảo toàn khối lượng ta được:
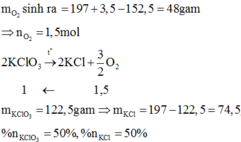

mgiảm = mO2 (sinh ra) = 200 + 3 - 145,4 = 57,6 (g)
\(\rightarrow n_{O_2}=\dfrac{57,6}{32}=1,8\left(mol\right)\)
PTHH: 2KClO3 --to, MnO2--> 2KCl + 3O2
1,2 1,8
\(\rightarrow m_{KClO_3}=1,2.122,5=147\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{147}{200}=73,5\%\\\%m_{KCl}=100\%-73,5\%=26,5\%\end{matrix}\right.\)
Khối lượng oxi thoát ra: 197 + 3 – 152 = 48(g)
Số mol O2=4832=1,5(mol)O2=4832=1,5(mol)
Phương trình hóa học của phản ứng :
2KClO3MnO2,to⟶2KCl+3O22KClO3⟶MnO2,to2KCl+3O2
2 mol 3 mol
1,5×23=1mol1,5×23=1mol ←← 1,5 mol
Khối lượng KClO3KClO3 trong hỗn hợp : 1 x 122,5 =122,5 (g)Khối lượng KCl trong hỗn hợp ban đầu: 197 – 122,5 = 74,5(g)→%mKClO3=62,18%;%mKCl=37,82%→%mKClO3=62,18%;%mKCl=37,82%

Đáp án A.
Bảo toàn khối lượng: mO2 = 3 + 197 – 152 = 48 (gam)
nO2 = 1,5 (mol)
2KClO3 → 2KCl + 3O2 ↑
⇒ mKCl = 197 – 1.122,5 = 74,5 (gam)