Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{O_2}=\dfrac{22,12-21,16}{32}=0,03\left(mol\right)\)
\(n_{KMnO_4}=\dfrac{22,12}{158}=0,14\left(mol\right)\)
Mn+7 + 5e --> Mn+2
0,14-->0,7
2O-2 - 4e --> O20
0,12<--0,03
2Cl- - 2e --> Cl20
2a<---a
Bảo toàn e: 2a + 0,12 = 0,7
=> a = 0,29 (mol)
=> VCl2 = 0,29.22,4 = 6,496 (l)

Sơ đồ phản ứng:
KMnO4--(t0) ->{K2MnO4 ,MnO2 ,O2; KMnO4 dư --(HCl)--> KCl; MnCl2,Cl2, H2O.
nKMnO4=25,28/158=0,16 mol ;
Bảo toàn khối lượng---> nO thoát ra = (25,28-23,52)/16=0,11 mol;
Bảo toàn O --> nO còn lại= 0,16*4-0,11=0,53 mol;
--> nH2O = 0,53 mol;
Bảo toàn H --> nHCl = 2nH2O= 2* 0,3 =1,06 (mol);
Bảo toàn K --> nKCl= nKMnO4= 0,16 mol;
Bảo toàn Mn--> nMnCl2=nKMnO4=0,16 mol;
Bảo toàn Cl:
nHCl =nKCl + 2* nMnCl2 + 2*nCl2;
--> nCl2=(1,06 -0,16 -0,16*2 )/2=0,29 mol
--> V =0,29*22,4=6,496(mol)

\(H_2S + CuSO_4 \to CuS + H_2SO_4\\ n_{H_2S} = n_{CuS} = \dfrac{1,44}{96} = 0,015(mol)\\ FeS + 2HCl \to FeCl_2 + H_2S\\ Fe + 2HCl \to FeCl_2 + H_2\\ Fe + S \xrightarrow{t^o} FeS\\ n_{Fe\ dư} = n_{H_2} = \dfrac{0,784}{22,4} - 0,015 = 0,02(mol)\\ n_{FeS} = n_{H_2S} = 0,015(mol)\\ \Rightarrow n_{Fe} = n_{Fe\ dư} + n_{FeS} = 0,02 + 0,015 = 0,035(mol)\\ \Rightarrow n_S = n_{FeS} = 0,015(mol)\\ \Rightarrow m = 0,035.56 + 0,015.32 = 2,44(gam)\)

Z gồm : \(H_2(a\ mol) ; H_2S(b\ mol)\)
\(n_Z = a + b = \dfrac{5,6}{22,4} = 0,25(mol)\\ m_Z = 2a + 34b = 0,25.2.7,4 = 3,7(gam)\\ \Rightarrow a = 0,15 ; b = 0,1\\ ZnS + 2HCl \to ZnCl_2 + H_2S\\ Zn + 2HCl \to ZnCl_2 + H_2\\ Zn + S \xrightarrow{t^o} ZnS\\ n_{Zn} = n_{ZnS} + n_{Zn\ dư} = n_{H_2S} + n_{H_2} = 0,25(mol)\\ n_S = n_{H_2S} = 0,1(mol)\\ \Rightarrow m = 0,25.65 + 0,1.32 = 19,45(gam)\)

Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.

Đáp án B
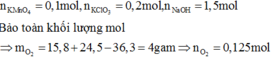
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
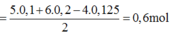


2KMnO4-to-> K2MnO4 + MnO2 + O2
nKMnO4= 22.12/158=0.14 (mol)
=> nK2MnO4= 0.07 (mol) => mK2MnO4= 13.79g
=> nMnO2= 0.07 (mol) => mMnO2= 6.09g
mhhr= 13.79+6.09=19.88g< 22.12g => KMnO4 dư
Đặt: nKMnO4(pư)=x (mol)
mhhr= mKMnO4 (dư) + mK2MnO4 + mMnO2= 22.12 - 158x+ 0.5x197+ 0.5x87=21.16
=> x= 0.06
2KMnO4 + 16HCl(đ) -to-> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
=> nCl2= 0.06*5/2= 0.15 (mol)
VCO2= 0.15*22.4=3.36l
Chúc bạn học tốt <3
Bạn ơi mình không hiểu lấy 0,5 ở đâu