Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Các phương trình phản ứng điều chế các khí:
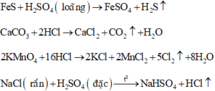
Khí X được thu bằng phương pháp đẩy nước, do đó X phải không tan hoặc ít tan trong nước
Vậy X không thể là HCl vì HCl tan nhiều trong nước

Chọn đáp án B
Trong phòng thí nghiệm ta chỉ cần lượng nhỏ nên cần phải dùng phương pháp điều chế nhanh và dễ dàng.Còn trong công nghiệp thì yêu cầu là ít tốn kém và thu được lượng lớn.
Chú ý : Theo mình nghĩ câu này cả B và C đều hợp lý.

Viết các PTHH :
H 2 SO 4 + CuO → CuSO 4 + H 2 O (1)
2 H 2 SO 4 + Cu → CuSO 4 + SO 2 + 2 H 2 O (2)
Theo (1): Muốn điều chế được 1 mol CuSO 4 cần 1 mol H 2 SO 4
Theo (2): Muốn điều chế được 1 mol CuSO 4 cần 2 mol 2 H 2 SO 4
Kết luận : Phương pháp thứ nhất tiết kiệm được một nửa lượng axit sunfuric.

Đáp án A.
Các thí nghiệm 1,4,5.
O3 + 2KI + H2O → 2KOH + I2 + O2
2KClO3 → 2KCl + 3O2
2H2S + SO2 →3S + 2H2O

Đáp án C.
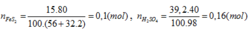
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

Đáp án C
Trong phòng thí nghiệm, khí clo được điều chế bằng cách cho axit clohidric đặc tác dụng với chất oxi hoá mạnh như mangan đioxit rắn (MnO2), KMnO4 hoặc KClO3…
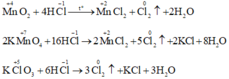

Đáp án A
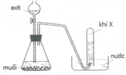
Khí X thu bằng phương pháp đẩy không khí khi để ống nghiệm úp ngược, do đó X phải nhẹ hơn không khí.
Trong các khí ta thấy:
H 2 (M=2) nhẹ hơn không khí (M=29)
CO 2 ( M = 44 ) , Cl 2 ( M = 17 ) , NO 2 ( M = 46 ) nặng hơn không khí (M=29)
Vậy khí X là H2.

Để khí clo thoát ra nhanh hơn thì dùng HCl đặc (nồng độ cao) đun nhẹ hỗn hợp (tăng nhiệt độ phản ứng). Chọn A

Do Na2SO3 còn tính khử nên không dùng axit nitric, nếu không sẽ tạo ra khí khác
axit sunfuric H2S rất yếu; axit clohiđic: sợ lẫn khí HCl
Vậy nên dùng H2SO4 là tốt nhất