Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH :\(Al+4HNO_3-->Al\left(NO_3\right)_3+NO\uparrow+2H_2O\) (1)
\(3Cu+8HNO_3-->3Cu\left(NO_3\right)_2+2NO\uparrow+4H_2O\) (2)
Đặt \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\) => 27x + 64y = 7,5 (*)
Theo PTHH (1) và (2) : \(\Sigma n_{NO}=n_{Al}+\dfrac{2}{3}n_{Cu}\)
=> \(\dfrac{3,36}{22,4}=0,15=x+\dfrac{2}{3}y\) (**)
Từ (*) và (**) suy ra : x = 0,1 ; y = 0,075
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{27\cdot0,1}{27\cdot0,1+64\cdot0,075}\cdot100\%=36\%\\\%m_{Cu}=100\%-36\%=64\%\end{matrix}\right.\)

Phần O2 sinh ra khi nung đi hết vào kim loại tạo oxit, đó là lý do ta chỉ thu được một khí Z là NO2 (0,4 mol).
Khi nung hỗn hợp T trong không khí thì sản phẩm thu được sẽ gồm các oxit “bão hòa” hóa trị (CuO, Fe2O3).
Số mol electron tối đa mà X có thể cho là: 3nNO =0,54 mol
Như vậy sẽ cần 0,54/2 = 0,27 mol O đưa vào rắn X để thu được 41,6 gam rắn gồm các oxit “bão hòa”.
→mX = mr + mO = 41,6 -0,27.16=37,28 gam
→m =mX = mNO2 = 37,28+46x0,4=55,68 gam
Chọn đáp án A

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B

Ta có: nFe=0,02 mol; nCu= 0,03 mol, nH2SO4= 0,2 mol, nNaNO3= 0,08 mol
nH+= 2n H 2 S O 4 = 0,4 mol, n N O 3 -= 0,08 mol
3Cu + 8H+ + 2NO3-® 3Cu2+ + 2NO + 4H2O (1)
0,03 0,08 0,02 ® 0,03 mol
Fe + 4H+ + NO3- ® Fe3+ + NO + 2H2O (2)
0,02 0,08 0,02 ® 0,02 mol
Tổng số mol H+ tham gia phản ứng (1) và (2) là 0,08+ 0,08= 0,16 mol
→nH+ dư= 0,4-0,16= 0,24 mol
Dung dịch X có chứa Cu2+, Fe3+ và H+
H++ OH-→H2O (3)
Cu2++ 2OH- → Cu(OH)2 (4)
Fe3++ 3OH- → Fe(OH)3 (5)
Theo PT (3), (4), (5) ta có
nOH-= nH++ 2nCu2++ 3nFe3+= 0,24+ 2.0,03+ 3.0,02= 0,36 mol= nNaOH
→V= 0,36 lít= 360 ml
Đáp án A

Suy luận:
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: 4V1 ← V1 lít
TN2: 8V1 ← 2V1 lít
Nhận thấy: nH+ (TN2)= 2nH+ (TN1) → (1) là KNO3; (2) là HNO3; (3) là H2SO4
3Cu+ 8H++ 2NO3- → 3Cu2++ 2NO + 4 H2O
TN1: ban đầu 5.10-3 10.10-3
Phản ứng 5.10-3 1,25.10-3
TN3: ban đầu 15.10-3 5.10-3
Phản ứng 15.10-3 3,75.10-3
Các thể tích khí đo ở cùng điều kiện nên nNO(TN3)= 3nNO (TN1) → VNO(TN3)= 3VNO (TN1) hay V2= 3 V1
Đáp án B



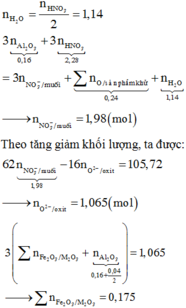
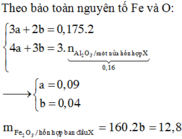
I)
1) CuO + CO --to--> Cu + CO2
2) CO2 + Ca(OH)2 ---> CaCO3 + H2O
3) NaHCO3 + NaOH ---> Na2CO3 + H2O
4) Ca(HCO3)2 + 2KOH ---> CaCO3 + K2CO3 + 2H2O
II) \(n_{H_3PO_4}=0,05.1=0,05\left(mol\right)\)
PTHH: 2NaOH + H3PO4 ---> Na2HPO4 + 2H2O
0,1<----0,05--------->0,5
=> \(\left\{{}\begin{matrix}V=V_{ddNaOH}=\dfrac{0,1}{1}=0,1\left(l\right)=100\left(ml\right)\\m_{muối}=m_{Na_2HPO_4}=0,05.142=7,1\left(g\right)\end{matrix}\right.\)
III)
NH4Cl + AgNO3 ---> AgCl + NH4NO3
NaBr + AgNO3 ---> AgBr + NaNO3
Cu(NO3)2 + 2NaOH ---> Cu(OH)2 + 2NaNO3
IV)
Gọi nCu = a (mol); nAl = b (mol)
=> 64a + 27b = 15 (1)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Quá trình oxi hóa, khử:
Cu0 ---> Cu+2 + 2e
a---------------->2a
Al0 ---> Al+3 + 3e
b--------------->3b
N+5 + 3e ---> N+2
0,9<----0,9
BTe: 2a + 3b = 0,9 (2)
Từ (1), (2) => a = 0,15; b = 0,2
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,15.64}{15}.100\%=64\%\\\%m_{Al}=100\%-64\%=36\%\end{matrix}\right.\)