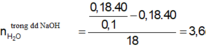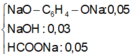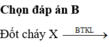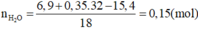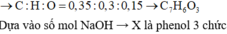Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
Đặt nNaOH pứ = x => nNaOH dư = 0,2x => nNaOH = 1,2x
Bảo toàn Na : 1,2x = 0,09.2 => x = 0,15
=> nNaOH pứ = 3nX => 3 thành phần phản ứng (este + phenol)
nNaOH dư = 0,03 mol
nC = 0,26 + 0,09 = 0,35 mol => Số C trong muối = 0,35 : 0,05 = 7
nH = 0,14.2 = 0,28 => 0,03 + (Số H trong muối).0,05 = 0,28 => H = 5
Số Na trong muối là 0,15 : 0,05 = 3
=> Y có : 0,05 mol C7H5OaNa3 ; 0,03 mol NaOH dư
=> mY = 0,05.(158 + 16a + 1,2 = 9,1 + 0,8a
Lập bảng :
a = 3 => mY = 11,5g
a = 4 => mY = 12,3g (TM)
a = 5 => mY = 13,1g

Chọn đáp án D.
Y + O2 → 0,15 mol Na2CO3 + 0,55 mol CO2 + 0,25 mol H2O
→ B T N T N a n N a O H = 2 n N a 2 C O 3 = 0 , 3 m o l
=> Khối lượng nước trong dung dịch NaOH = 88g
=> Lượng nước sinh ra từ phản ứng = 91 , 6 - 88 18 = 0 , 2 mol
0,1 mol X + vừa đủ 0,3 mol NaOH → 0,2 mol H2O
=> Chứng tỏ X là este của phenol, trong vòng benzen có gắn 1 nhóm -OH.
=> X có chứa 3 nguyên tử O
=> n O X = 0 , 3 mol
=> Trong X: n C : n H : n O = 7 : 8 : 3
=> CTPT của X là C7H8O3.
=> CTCT của X là HCOOC6H4OH.
⇒ m = m H C O O N a + m N a O C 6 H 4 O N a = 22 , 2 g

Đáp án : D
Khi đốt cháy X : Bảo toàn khối lượng : mX + mO2 = mCO2 + mH2O
=> nH2O = 0,15 mol ; nCO2 = 0,35 mol ; nO2 = 0,35 mol
Bảo toàn O : nO(X) = 2nCO2 + nH2O – 2nO2 = 0,15 mol
=> nC : nH : nO = 0,35 : 0,3 : 0,15 = 7 : 6 : 3
=> X có công thức trùng với công thức đơn giản nhất là C7H6O3 chứa 1 vòng benzen. Có (pi + vòng) = 5 => có 1 pi ở ngoài vòng
,nX = 0,05 mol ; nNaOH pứ = 0,15 mol = 3nX
=> X phải là HCOOC6H4OH phản ứng tạo : HCOONa ; C6H4(ONa)2
Sau phản ứng có 0,05 mol HCOONa ; 0,05 mol C6H4(ONa)2 ; 0,03 mol NaOH
=> m = 12,3g

n CO =a
n CO2=b
a+b=0,2
28a +44b=8
=>a=0,05
b=0,15
FexOy +yCO-to->xFe +yCO2
0,15/y <= 0,15
8=(56x +16y).0,15/y
=> x/y=2/3
=> Fe2O3