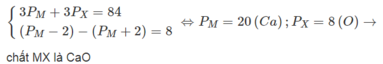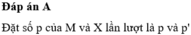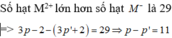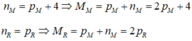Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có:
\(\left\{{}\begin{matrix}2\left(Z_{X^{2-}}+Z_{M^{2+}}\right)+\left(N_{X^{2-}}+N_{M^{2+}}\right)=84\\2\left(Z_{X^{2-}}+Z_{M^{2+}}\right)-\left(N_{X^{2-}}+N_{M^{2+}}\right)=28\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}Z_{X^{2-}}+Z_{M^{2+}}=28\\N_{X^{2-}}+N_{M^{2+}}=28\end{matrix}\right.\left(1\right)\)
Lại có: \(\left\{{}\begin{matrix}A_{X^{2-}}-A_{M^{2+}}=8\\S_{X^{2-}}-S_{M^{2+}}=16\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}\left(Z_{X^{2-}}+N_{X^{2-}}\right)-\left(Z_{M^{2+}}+N_{M^{2+}}\right)=8\\\left(2Z_{X^{2-}}+N_{X^{2-}}\right)-\left(2Z_{M^{2+}}+N_{M^{2+}}\right)=16\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}\left(Z_{X^{2-}}-Z_{M^{2+}}\right)+\left(N_{X^{2-}}-N_{M^{2+}}\right)=8\\2\left(Z_{X^{2-}}-Z_{M^{2+}}\right)+\left(N_{X^{2-}}-N_{M^{2+}}\right)=16\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}Z_{X^{2-}}-Z_{M^{2+}}=8\\N_{X^{2-}}-N_{M^{2+}}=0\end{matrix}\right.\left(2\right)\)
Từ (1) và (2) ta có:\(\left\{{}\begin{matrix}N_{X^{2-}}+N_{M^{2+}}=28\\Z_{X^{2-}}+Z_{M^{2+}}=28\\N_{X^{2-}}-N_{M^{2+}}=0\\Z_{X^{2-}}-Z_{M^{2+}}=8\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z_{X^{2-}}=18\\N_{X^{2-}}=14\\Z_{M^{2+}}=10\\N_{M^{2+}}=14\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}Z_X=16\\N_X=16\\Z_M=12\\N_M=12\end{matrix}\right.\)
Vậy X là Lưu huỳnh, M là Magie => MX là MgS

Gọi số p,e,n trong của M và X lần lượt là p1,e1,n1 , p2,e2,n2
=> 2(p1+e1+n1) + ( p2+e2+n2)=140
Mà số p=số e
=> 2(2p1 + n1) + ( 2p2 + n2) = 140 <=> (4p1+2p2) + (2n1+n2)=140 (I)
Lại có : (4p1+2p2)-(2n1+n2)=44 (II)
Từ (I) và (II ) => \(\left\{{}\begin{matrix}4p1+2p2=92\left(1\right)\\2n1+n2=48\end{matrix}\right.\)
Lại có : (p1 + n1) - (p2+n2)=23 (III)
(2p1 + n1 -1) - (2p2+n2+2) =31 (IV)
Từ (III) và (IV) => \(\left\{{}\begin{matrix}p1-p2=11\left(2\right)\\n1-n2=12\end{matrix}\right.\)
Từ (1) và (2) => \(\left\{{}\begin{matrix}p1=19\\p2=8\end{matrix}\right.\)
=> số e của M là 19 e
số e của X là 8 e
=> cấu hình e của M là : 1s22s22p63s23p64s1
cấu hình e của X là : 1s22s22p4

Đáp án C.
Gọi p, e, n là số proton, số electron và số nơtron trong một nguyên tử M; p’, e’, n’ là số proton, số electron và số nơtron trong một nguyên tử X.
Trong nguyên tử số proton = số electron; các hạt mang điện là proton và electron, hạt không mang điện là nơtron.
+ Trong phân tử của M2X2 có tổng số hạt proton, nơtron và electron là 164 nên suy ra:
2(2p + n) + 2(2p’ + n’) = 164 (1)
+ Trong đó số hạt mang điện nhiều hơn hạt không mang điện là 52 nên suy ra:
(4p + 4p’) - 2(n + n’) = 52 (2)
+ Số khối của M lớn hơn số khối của X là 23 đơn vị nên ta có suy ra:
(p + n) - (p’ + n’) = 23 (3)
+ Tổng số hạt electron trong M+ nhiều hơn trong X22- là 7 hạt nên suy ra:
(2p + n - 1) - 2(2p’ + n’) + 2 = 7 (4)
Giải hệ (1), (2), (3), (4) ta được p = 19 ⇒ M là kali; p’ = 8 ⇒ X là oxi.
Công thức phân tử của hợp chất là K2O2.

Đáp án C.
Tổng số hạt trong phân tử Y là 214 hạt.
4(2pM + nM) + 3(2pX + nX) = 214 (1)
Ion M3+ có số electron bằng số electron của ion X4 −
pM - 3 = pX + 4 => pX = pM - 7 (2)
Tổng số hạt proton, nơtron, electron của nguyên tử nguyên tố M nhiều hơn tổng số hạt của nguyên tử nguyên tố X trong Y là 106
4(2pM + nM) - 3(2pX + nX) = 106 (3)
(1), (3) => 2pM + nM = 40 (4) và 2pX + nX = 18 (5)
(5),(2),(4) => pX = 6 ; pM = 13 => X là C (Carbon) và M là Al (Nhôm)
Y la Al4C3 (Nhôm carbua)

M chiếm 52,94% về khối lượng:
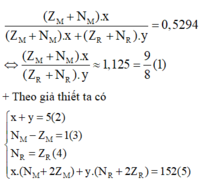
Quan sát – phân tích: Để tìm câu trả lời cho bài toán ta chỉ cần xác định được 4 ẩn x;y; Z M ; Z R
Vì vậy ta sẽ tìm cách khử các ẩn không cần thiết bằng cách thế phương trình (3) và (4) lầ lượt vào phương trình (1) và (5):
Thế (3) và (4) vào phương trình (1) ta được:
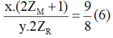
Thế (3) và (4) vào phương trình (5) ta được:
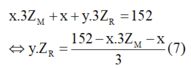
Quan sát – phân tích: Ba phương trình (2); (6); (7) với 4 ẩn ta nghĩ ngay đến biện luận để tìm nghiệm.
Thế (7) vào (6) ta được
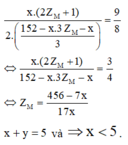
Mặt khác x nguyên
x nhận các giá trị 1, 2, 3, 4
Ta có bảng sau:
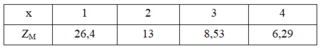
=> Cặp nghiệm thỏa mãn: x = 2 và Z M = 13 ⇒ M là Al
Thay x và ZM vào (7) và (2) ta tìm được y =3 và Z R = 8 ⇒ R là Oxi
Do đó hợp chất X là Al2O3 tổng số proton trong X là 13.2 + 8.3 = 50
Đáp án B.

Gọi số notron và proton của M lần lượt là n1,p1
số n và p của X là n2,p2
Theo đề bài ta có: p1+2p2=58 (1)
Vì me rất nhỏ => M=n+p
do đó: n1+p1=M của M
n2+p2= M của X
=>n1+p1=46,67%(n1+p1+2n2+2p2)
hay n1+p1=7/8(2n2+2p2)
có n1=p1+4 và n2=p2
nên 4p1+8=7p2 (2)
(1),(2) => p1=26,n1=30
Vậy M là Fe