Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

câu 1
gọi CT NxHy
ta có
x: y = \(\frac{82,35}{14}:\frac{17,65}{1}\) = 1: 3
=> NH3

dA/O2=\(\dfrac{M_A}{32}\)=0,5 => MA=16g/mol
mC=\(\dfrac{75}{100}.16\)=12g =>nC=\(\dfrac{12}{12}\)=1 mol
mH=16-12=4g/mol =>nO=\(\dfrac{4}{1}\)=4 mol
CTHH của A là CH4

1
\(MP_2O_3=110g/mol\)
\(\%P=\dfrac{31.2.100}{110}=58,2\%\)
\(\%O=100-58,2=41,8\%\)
2
\(MA=8.2=16g/mol\)
Tính theo hoá trị
=> cthh của A là CH\(_4\)

\(M_A=8.M_{H_2}=8.2=16(g/mol)\)
Trong 1 mol A: \(\begin{cases} n_C=\dfrac{16.75\%}{12}=1(mol)\\ n_H=\dfrac{16.25\%}{1}=4(mol) \end{cases}\)
Vậy \(CTHH_A:CH_4\)

bài1
ta có dA/H2=22 →MA=22MH2=22 \(\times\) 2 =44
nA=\(\frac{5,6}{22,4}\)=0,25
\(\Rightarrow\)mA=M\(\times\)n=11 g
MA=dA/\(H_2\)×M\(H_2\)=22×(1×2)=44g/mol
nA=VA÷22,4=5,6÷22,4=0,25mol
mA=nA×MA=0,25×44=11g

Ta có : dA/H2 = MA/MH2 = MA/2 = 8
=> MA = 2.8 = 16 (g/mol)
mC = 16.75:100 = 12 (g)
mH = 16.25:100 = 4 (g)
=> nC = mC:MC = 12:12 = 1 (mol)
nH = mH:MH = 4:1 = 4 (mol)
Đặt công thức dạng chung của hợp chất A là : CxHy
x = nC = 1
y = nH = 4
Vậy CTHH là : CH4
CHÚC BẠN HỌC TỐT NHA !
các bạn giúp mình trả lời câu hỏi của mình với
THANK YOU VERY MUCH

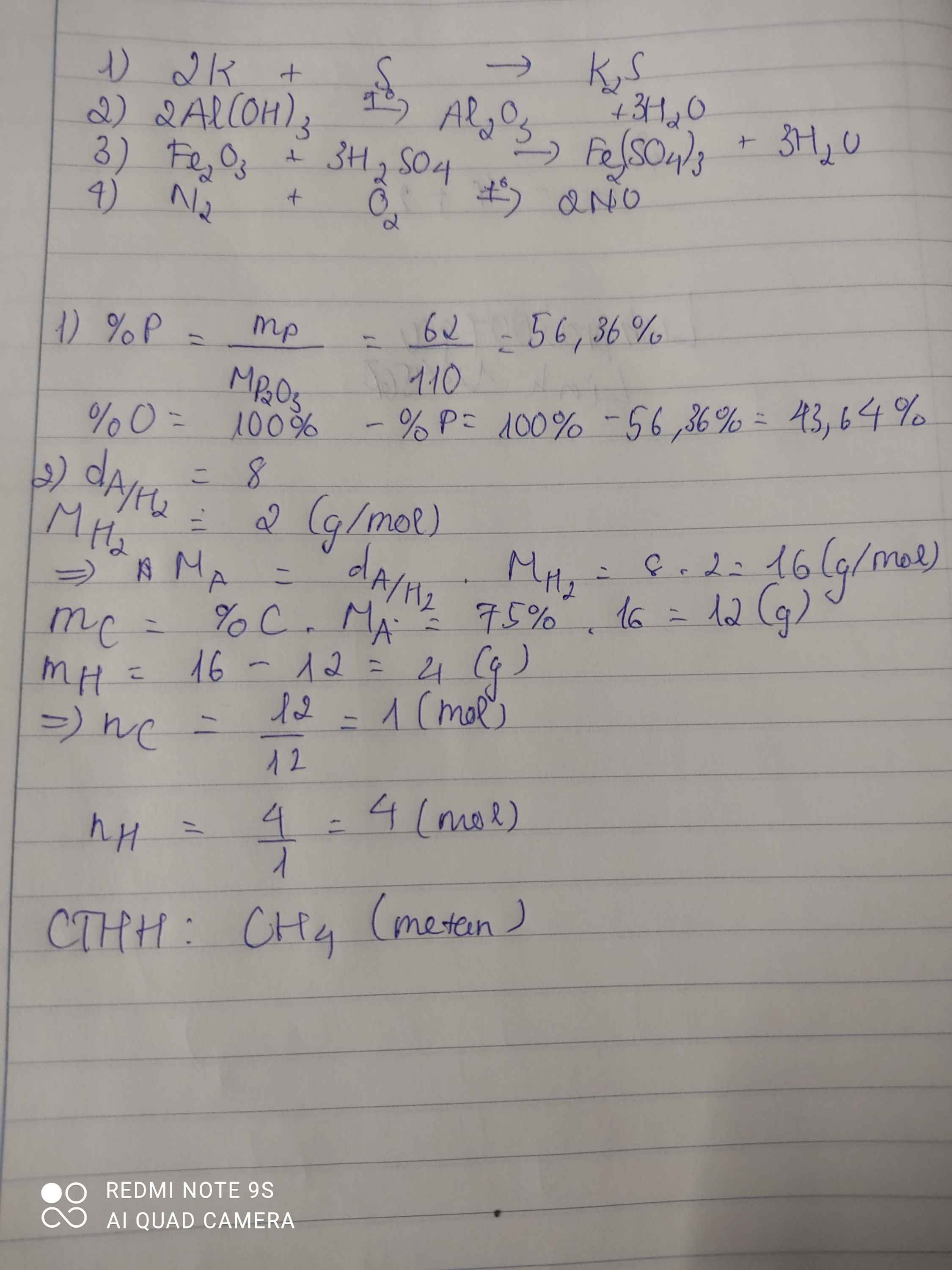
Viết CTHH có dạng \(C_xH_y\)
Ta có dA/O2=\(\dfrac{M_A}{M_{O2}}\)
<=> 0,5=\(\dfrac{M_A}{32}\)
=>\(M_A\)=32*0,5=16(g)
\(m_C\)=\(\dfrac{\%C\cdot M_A}{100\%}\)=\(\dfrac{75\%\cdot16}{100\%}\)=12(g)
\(n_C\)=\(\dfrac{m_C}{M_C}=\dfrac{12}{12}=1\)(mol)
->x=1
\(m_H=16-12=4\left(g\right)\)
\(n_H=\dfrac{m_H}{M_H}=\dfrac{4}{1}=4\left(mol\right)\)
->y=4
Vậy CTHH là \(CH_4\)