Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì A và B là hiđrocacbon nên khi đốt cháy chỉ thu được CO2 và H2O.
Ta có: \(n_{O_2}=\dfrac{64}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
BTNT O, có: \(n_{H_2O}=2n_{O_2}-2n_{O_2\left(dư\right)}-2n_{CO_2}=1,6\left(mol\right)\)
Có: nH2O > nCO2 nên A và b là ankan.
⇒ nankan = nH2O - nCO2 = 0,6 (mol)
Giả sử CTPT chung của A và B là: \(C_{\overline{n}}H_{2\overline{n}+2}\).
Có: n = số nguyên tử C = \(\dfrac{1}{0,6}=1,67\)
Mà: A và B là 2 ankan kế tiếp.
Nên A và B lần lượt là CH4 và C2H6.
Bạn tham khảo nhé!

Ta có: \(n_{O_2\left(banđau\right)}=\dfrac{62}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí thoát ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
\(\Rightarrow n_{O_2\left(pư\right)}=2-0,2=1,8\left(mol\right)\)
BTNT O, có: \(2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=2.1,8-2.1=1,6\left(mol\right)\)
Vì đốt cháy 2 hiđrocacbon thu được nH2O > nCO2 nên A và B là ankan.
⇒ nankan = 1,6 - 1 = 0,6 (mol)
Gọi CTPT chung của A và B là \(C_{\overline{n}}H_{2\overline{n}+2}\)
\(\Rightarrow\overline{n}=\dfrac{1}{0,6}=1,667\)
Vậy: A và B là CH4 và C2H6.
Bạn tham khảo nhé!

Đặt :
nX = nY = x (mol)
CT : CnH2n+2 , CmH2m+2
nCO2 = 13.44/22.4 = 0.6 (mol)
BT C :
x(n+m) = 0.6 (1)
mhh = x(14n + 2) + x(14m + 2) = 8.8
=> 14x(n+m) + 4x = 8.8
=> 14*0.6 + 4x = 8.8
=> x = 0.1
Từ (1) => n + m = 0.6/0.1 = 6
BL : n = 2 , m = 4 => C2H6 , C4H8
n = 1 , m = 5 => CH4 , C5H12

Đáp án A
Phương pháp: Khi dẫn qua dung dịch Br2, C3H6 và C2H4 phản ứng
nBr2 = nC3H6 + nC2H4
mbình tăng = mC3H6 + mC2H4
Bảo toàn nguyên tố C, H, O.
Hướng dẫn giải:
Khi dẫn qua dung dịch Br2, C3H6 (x mol) và C2H4 (y mol) bị giữ lại.
x + y = nBr2 = 4/160 = 0,025 mol
42x+28y = m bình tăng = 0,91
Giải hệ ta tìm được x = 0,015 mol; y = 0,01 mol
nY = 54,545%nX = 54,545% (0,025 + nY) => nY = 0,03 mol;
Y gồm: CH4: 0,015 mol; C2H6: 0,01 mol; C4H10 dư: 0,03 – 0,015 – 0,01 = 0,005 mol
+ BTNT C: nCO2: 0,015+0,01.2+0,005.4 = 0,055 mol
+ BTNT H: nH2O: 0,015.2+0,01.3+0,005.5 = 0,085 mol
BTNT O: nO2 = nCO2 + 0,5nH2O = 0,055 + 0,5.0,085 = 0,0975 mol
VO2 = 2,184 lít.

Đáp án A
Khi dẫn qua dung dịch Br2, C3H6 (x mol) và C2H4 (y mol) bị giữ lại.
x + y = nBr2 = 4/160 = 0,025 mol
42x+28y = m bình tăng = 0,91
Giải hệ ta tìm được x = 0,015 mol; y = 0,01 mol
nY = 54,545%nX = 54,545% (0,025 + nY) => nY = 0,03 mol;
Y gồm: CH4: 0,015 mol; C2H6: 0,01 mol; C4H10 dư: 0,03 – 0,015 – 0,01 = 0,005 mol
+ BTNT C: nCO2: 0,015+0,01.2+0,005.4 = 0,055 mol
+ BTNT H: nH2O: 0,015.2+0,01.3+0,005.5 = 0,085 mol
BTNT O: nO2 = nCO2 + 0,5nH2O = 0,055 + 0,5.0,085 = 0,0975 mol
VO2 = 2,184 lít.

Đáp án C
Ta có mBình tăng = mCO2 + mH2O = 13,3 gam.
Với nCO2 = nBaCO3 = 0,2 mol ||⇒ nH2O = 0,25 mol.
Nhận thấy nC ÷ nH = 0,2 ÷ (0,25×2) = 2 ÷ 5

Đáp án D
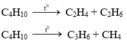
Khí hỗn hợp qua bình đựng Br2 ta có:

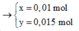
Ta có
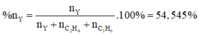
→ n Y = 0 , 03 m o l
Hỗn hợp Y gồm:
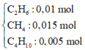
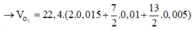
= 2,184 (L)

Đáp án A
Từ giả thiết suy ra :
n C O 2 = n C a C O 3 = 100 100 = 1 m o l ; n O 2 p ư = n O 2 b đ - n O 2 d ư = 64 32 - 11 , 2 . 0 , 4 0 , 082 . 273 = 1 , 8 m o l .
Đặt công thức phân tử trung bình của A và B là C n ¯ H 2 n ¯ + 2
Phương trình phản ứng cháy:
C n ¯ H 2 n ¯ + 2 + 3 n ¯ + 1 2 O 2 → n ¯ C O 2 + ( n ¯ + 1 ) H 2 O ( 1 ) m o l x → 3 n ¯ + 1 2 . x → n ¯ . x