Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

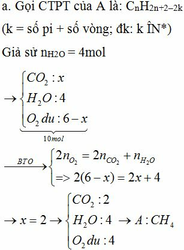
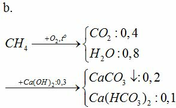
pt:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,3 → 0,3 0,3
CO2 + CaCO3 + H2O → Ca(HCO3)2
0,1 → 0,1 0,1
m dd tăng = mCO2 + mH2O – mCaCO3 = 12g

1) \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> nC = 0,3 (mol)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
\(n_A=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Số nguyên tử C = \(\dfrac{0,3}{0,1}=3\) (nguyên tử)
Số nguyên tử H = \(\dfrac{0,6}{0,1}=6\) (nguyên tử)
CTHH: C3H6
2)
PTHH: 2C3H6 + 9O2 --to--> 6CO2 + 6H2O
0,1--->0,45
=> mO2 = 0,45.32 = 14,4 (g)

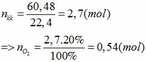
CH3OH và C2H5OH có CT chung là CnH2n+2O.
CH3OH và C2H5OH có cùng số mol nên:
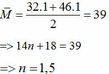
Vậy CT chung của 2 ancol là: C1,5H5O
2 axit có công thức phân tử là: C3H6O2 và C6H10O4
Nhận xét: C1,5H5O ; C3H6O2 và C6H10O4 đều có số nguyên tử C gấp 1,5 lần số nguyên tử O
Gọi số mol của CO2: x (mol) ; nH2O = y (mol)
=> nO (trong hh đầu) = 2/3 nC =2/3 nCO2 = 2x/3 (mol) ( Vì nguyên tử C gấp 1,5 lần số nguyên tử
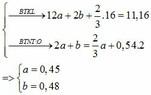
Khối lượng dung dịch giảm: ∆ = mCaCO3 – mCO2 – mH2O = 0,45.100 – 0,45.44 – 0,48.18 = 16,56 (g)

Tính % thể tích các khí :
% V C 2 H 2 = 0,448/0,896 x 100% = 50%
% V CH 4 = % V C 2 H 6 = 25%

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6
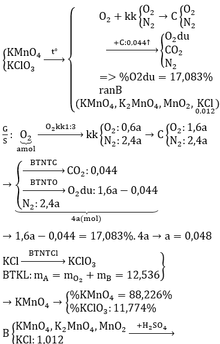
Hỗn hợp A gồm 2 hidrocacbon ở trạng thái khí là C2xHy và CxH2y (x, y ở 2 công thức có giá trị như nhau). Đốt trong bình kín hỗn hợp B gồm 1,12 lít A và 12,992 lít không khí (đktc). Sau khi 2 hidrocacbon cháy hết, làm ngưng tụ hoàn toàn hơi nước được hỗn hợp khí D.
Biết rằng: - Không khí có 20% thể tích oxi và 80% thể tích nitơ.
- Tỷ lệ khối lượng mol tương ứng của 2 hidrocacbon bằng 1,625.
- % thể tích N2 trong D nhiều hơn % thể tích N2 trong B là 12,275%.
Hỏi: a. Công thức phân tử của 2 hidrocacbon. b. % thể tích các khí trong A.
A gồm : X: C2xHy a mol và Y: CxH2y b mol => MX > MY
Vì là khí => 2x≤4=>x≤2
Mol A = a + b = 0,05. (1)
Mol không khí = 0,58 => mol O2 = 0,116 và mol N2 = 0,464
=> mol B = 0,05 + 0,58 = 0,63
%mol N2 trong B = 0,464*100/0,63 = 73,65
=> %mol N2 trong D = 73,65 + 12,275 = 85,93
=> mol D = 0,464/0,8593 = 0,54
D gồm :
N2: 0,464
CO2 = 2xa + xb
O2 dư = 0,116 - a(2x+0,25y)-b(x+0,5y)
=> mol D = mol N2 + mol CO2 + mol O2 dư = 0,54 => ay + 2by = 0,16. (2)
Với MX = 1,625*MY => 24x + y = 1,625(12x + 2y) => y = 2x
Nếu x = 2 => y = 4 => X: C4H4 và Y: C2H8 => loại
Nếu X = 1 => y = 2 => X: C2H2 và Y: CH4
(2) => a + 2b = 0,08. (3)
(1)(3) => a = 0,02 và b = 0,03
=> A gồm C2H2 40% và CH4 60%