Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2Al +6HCl-> 2AlCl3+3H2
0,6--------------------------0,9
Al2O3+6HCl-> 2AlCl3+3H2O
n H2=0,9 mol
=>m Al=0,6.27=16,2g
=>%mAl=\(\dfrac{16,2}{36,6}100\)=44,26%
=>%m Al2O3=55,74%
\(n_{H_2}=\dfrac{20,16}{22,4}=0,9mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,6 0,9
\(m_{Al}=0,6\cdot27=16,2g\)
\(\%m_{Al}=\dfrac{16,2}{36,6}\cdot100\%=44,26\%\)
\(\%m_{Al_2O_3}=100\%-44,26\%=55,73\%\)

\(n_{H_2}=\dfrac{20,16}{22,4}=0,9mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,6 0,9 ( mol )
( \(Al_2O_3+HCl\) không giải phóng \(H_2\) )
\(\rightarrow m_{Al}=0,6.27=16,2g\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{16,2}{36,6}.100=44,26\%\\\%m_{Al_2O_3}=100\%-44,26\%=55,74\%\end{matrix}\right.\)

Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4

\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,25 0,25 (Mol)
\(\Rightarrow n_{Zn}=0,25\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,25.65=16,25\left(g\right)\)
Chấ rắn không tan là Ag
\(\Rightarrow m_{Ag}=6,25\left(g\right)\)
\(\%m_{Zn}=\dfrac{16,25}{16,25+6,25}.100\%\approx72,22\%\)
\(\%m_{Ag}=\dfrac{6,25}{6,25+16,25}.100\%\approx27,78\%\)

RO+H2SO4→ RSO4+H2O (1)
RCO3+H2SO4→ RSO4+CO2+H2O (2)
Đặt a là khối lượng hỗn hợp X.
x,y là số mol RO và RCO3
Ta có : (R+16)x+(R+60)y=a (*)
Từ (1) và (2) \Rightarrow (R+96)(x+y)=1,68a (**)
Từ (2) \Rightarrow y=0,01a (***)
Giải (*),(**) và (***) \Rightarrow x=0,004a : R=24
Vậy R là Mg

a,Fe + 2HCl → FeCl + H2 (1)
FeO + 2HCl → FeCl + H2O (2)
nH2 = 3,36/ 22,4 = 0,15 ( mol)
Theo (1) nH2 = nFe = 0,15 ( mol)
mFe = 0,15 x 56 = 8.4 (g)
m FeO = 12 - 8,4 = 3,6 (g)
a, \(n_{H_2}=\frac{3,36}{22,4}=0,15\left(mol\right)\)
\(Fe+2HCl->FeCl_2+H_2\left(1\right)\)
\(FeO+2HCl->FeCl_2+H_2O\left(2\right)\)
theo (1) \(n_{Fe}=n_{H_2}=0,15\left(mol\right)\)
=> \(m_{Fe}=0,15.56=8,4\left(g\right)\)
=> \(m_{FeO}=12-8,4=3,6\left(g\right)\)

ta thấy : nFe =nH2 = 0,15
=> mFe =0,15 x 56 = 8,4g
%Fe=8,4/12 x 100 = 70%
=>%FeO = 100 - 70 = 30%
b) BTKLra mdd tìm mct of HCl
c) tìm mdd sau pứ -mH2 nha bạn
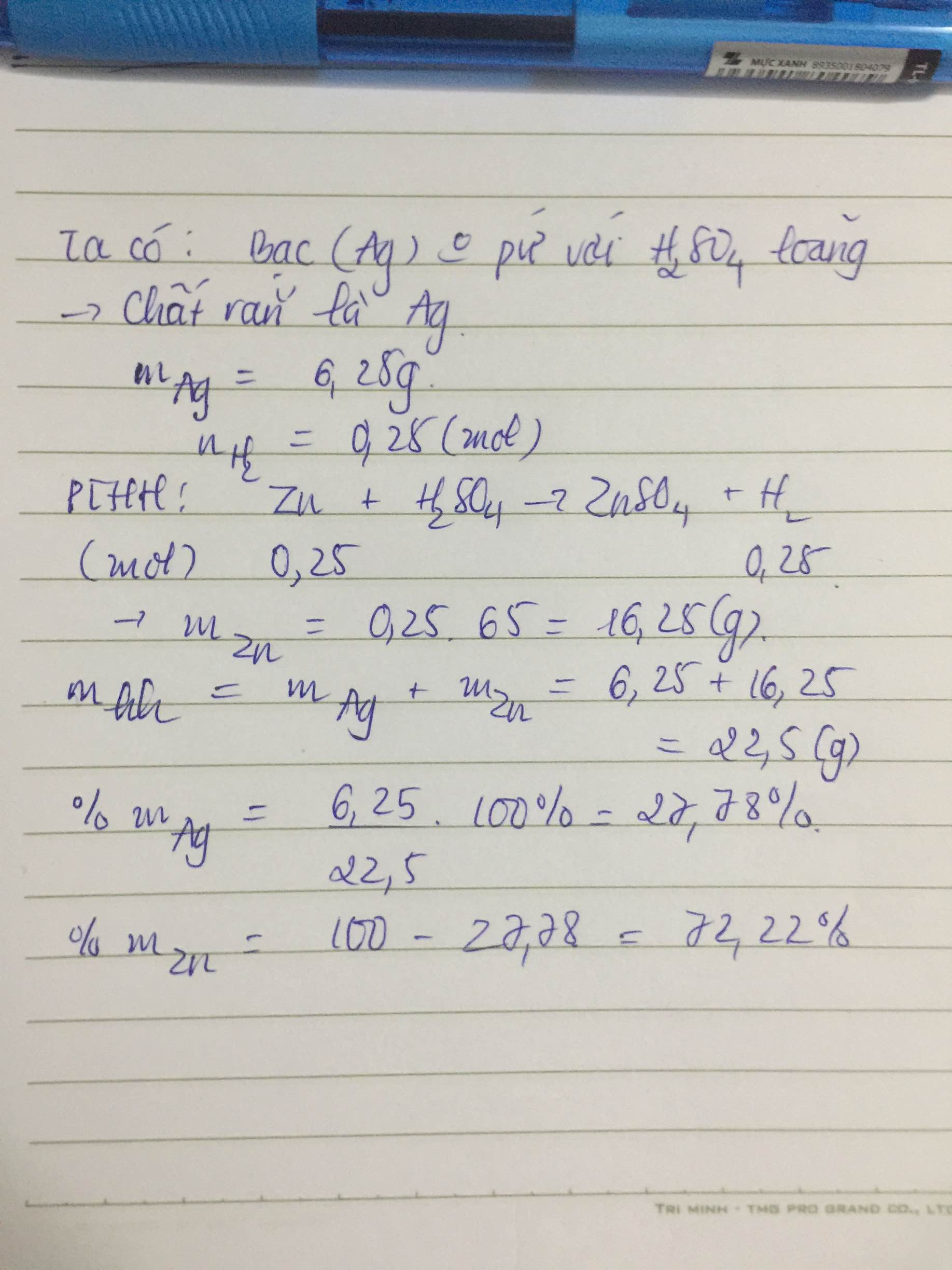


n NaCl = a(mol) ; n KCl = b(mol)
=> 58,5a + 74,5b = 0,325(1)
NaCl + AgNO3 → AgCl + NaNO3
KCl + AgNO3 → AgCl + KNO3
=> n AgCl = a + b = 0,717/143,5 (2)
Từ (1)(2) suy ra a = 0,003 ; b = 0,002
Suy ra
%m NaCl = 0,003.58,5/0,325 .100% = 54%
%m KCl = 100% -54% = 46%
Sửa đề: 0,717 thành 0,7175 cho số đẹp bạn nhé!
PT: \(NaCl+AgNO_3\rightarrow NaNO_3+AgCl_{\downarrow}\)
\(KCl+AgNO_3\rightarrow KNO_3+AgCl_{\downarrow}\)
Giả sử: \(\left\{{}\begin{matrix}n_{NaCl}=x\left(mol\right)\\n_{KCl}=y\left(mol\right)\end{matrix}\right.\)
⇒ 58,5x + 74,5y = 0,325 (1)
Ta có: \(n_{AgCl}=\dfrac{0,7175}{143,5}=0,005\left(mol\right)\)
Theo PT: \(n_{AgCl}=n_{NaCl}+n_{KCl}=x+y\left(mol\right)\)
⇒ x + y = 0,005 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{6400}\left(mol\right)\\y=\dfrac{13}{6400}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{NaCl}=\dfrac{\dfrac{19}{6400}.58,5}{0,325}.100\%\approx53,4\%\\\%m_{KCl}\approx46,6\%\end{matrix}\right.\)
Bạn tham khảo nhé!