Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B
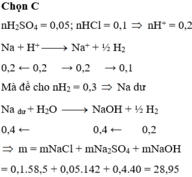
nH2SO4 = 0,05 mol ; nHCl = 0,1 mol ;
Lại có nH2 = 0,3 mol => 2nH2 > (2nH2SO4 + nHCl)
=> Na còn tác dụng với H2O
=> nNaOH = 2( nH2 – ½ nH+) = 0,4mol
=> Muối gồm : 0,05 mol Na2SO4 ; 0,1 mol NaCl ; 0,4 mol NaOH
=> mrắn khan = 28,95g

Chọn D.
Ta có: ![]()
Chất rắn gồm NaCl (0,1); Na2SO4 (0,05); NaOH (0,4) Þ m = 28,95 gam.

Chọn D
nH+ ban đầu = 0,2 mà nH2 = 0,2 Þ Ngoài phản ứng với H+ thì Na còn phản ứng với H2O
Þ Dung dịch sau cùng có n O H - = 0,2x2 - 0,2 = 0,2 (BTE)
mRắn = 0,2x2x23 + 0,05x96 + 0,1x35,5 + 0,2x17 = 20,95 gam.

Đáp án : A
, nH+ = 0,25 mol < 2nH2 = 2.0,15 = 0,3 mol
=> Kim loại còn phản ứng với H2O => nH2O pứ = 2nH2 pứ với nước = 0,3 – 0,25 = 0,05
Bảo toàn khối lượng : mKL + mH2O + mAxit = mrắn khan + mH2
=> mrắn khan = 19,475g

Đáp án : C
Dạng tổng quát : X + xHCl -> XClx + 0,5xH2
Do 2nH2 > nHCl => Kim loại phản ứng với H2O tạo OH‑
=> nCl(muối) = nHCl = 0,1 mol và nH2 (H2O) = 0,1 – nH2(HCl) = 0,05 mol
=> nOH = 2nH2(H2O) = 0,1 mol
=> m = mKL + mCl(muối) + mOH(bazo) = 9,95 + 0,1.35,5 + 0,1.17 = 15,2g

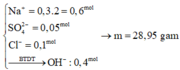

Chọn đáp án B
Ta có