Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Vì hai thí nghiệm đều thu được cùng một lượng kết tủa và lượng KOH dùng ở thí nghiệm 2 lớn hơn lượng KOH dùng ở thí nghiệm 1 nên ở thí nghiệm 1 chưa có sự hòa tan kết tủa và ở thí nghiệm 2, sau khi lượng kết tủa đạt giá trị cực đại đã bị hòa tan một phần.
Áp dụng công thức cho hai trường hợp cùng thu được một lượng kết tủa ta có hệ phương trình


TH1: Khi cho 0,48 mol NaOH thì chỉ tạo 1 phần kết tủa, khi cho 0,51 mol NaOH thì tạo kết tủa tối đa vào 1 phần bị tan
Trường hợp cho 0,51 mol NaOH
TH2: cả 2 lần đều tạo kết tủa tối đa và hòa tan 1 phần
Chênh lệch số mol kết tủa ở 2 trường hợp:
4
a
78
-
3
a
78
=
0
,
51
-
0
,
48
=
⇒
a
78
=
0
,
03
Trường hợp cho 0,48 mol NaOH
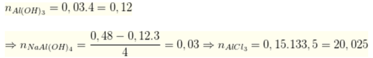
=>Đáp án C

Đáp án B
Khối lượng mỗi phần là 28,11/3 = 9,37g
Phần 2 tạo 0,04 mol CaCO3 => nCO32- = 0,04
Phần 1 tạo 0,11 mol CaCO3=> nHCO3- = 0,11 – 0,04 = 0,07
(2R + 60)0,04 + (R + 61)0,07 = 9,37 R = 18 R là NH4
Phần 3:
(NH4)2CO3 +2NaOH -> Na2CO3 + 2NH3 + 2H2O
NH4HCO3 + 2NaOH -> Na2CO3 + NH3 + 2H2O
nNaOH = (0,04 + 0,07).2 = 0,22 V = 0,22 lít

AlCl3 + KOH : 0,18 mol→ 0,06 mol Al(OH)3 + dd Y
DD Y + KOH : 0,21 mol → 0,03 mol Al(OH)3
Nhận thấy khi thêm KOH vào dung dịch Y lại tạo kết tủa
→ trong dung dịch Y còn AlCl3 còn dư : (0,1x- 0,06) mol
Vì 3×nKOH = 0,09 <nKOH = 0,21 mol → xảy ra hiện tượng hòa tan kết tủa
4nAlCl3 dư = nkết tủa + nKOH → nAlCl3 = (0,03 +0,21):4= 0,06 → 0,1x-0,06 = 0,06 → x= 1,2
Đáp án A
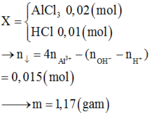


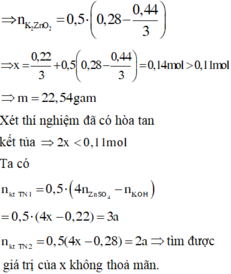
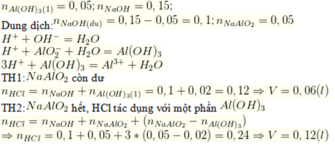
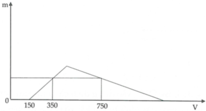

Chọn đáp án D