Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Hòa tan hoàn toàn m gam X thu được dung dịch Y và 0,45 mol H2.
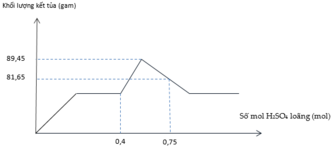
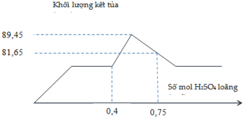
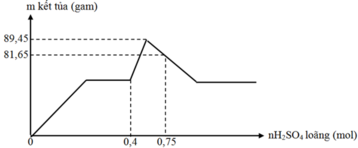
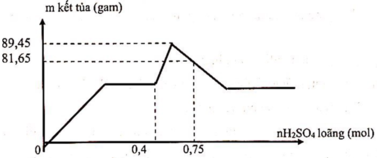
Do đồ thị như vậy nên giai đoạn đầu kết tủa tăng là do H2SO4 tác dụng với Ba(OH)2 tạo kết tủa BaSO4.
Giai đoạn kết tủa không đổi tiếp theo là H2SO4 trung hòa NaOH.
Giai đoạn kết tủa tăng lên do H2SO4 tác dụng với NaAlO2 tạo kết tủa Al(OH)3.
Giai đoạn kết tủa giảm do H2SO4 hòa tan Al(OH)3.
Giai đoạn kết tủa không đổi lúc này chỉ còn BaSO4
→ 2 n B a ( O H ) 2 + n N a O H = 0 , 4 . 2 = 0 , 8
Kết tủa tối đa là 89,45 gam gồm Al(OH)3 và BaSO4.
Lúc đạt 0,75 mol H2SO4 kết tủa bị giảm đi 7,8 gam tương đương với 0,1 mol Al(OH)3.
Lúc này lượng H2SO4 cần để hòa tan là 0,15 mol.
Vậy lúc kết tủa đạt cực đại thì lượng H2SO4 đã dùng là 0,6 mol
Trong giai đoạn tạo kết tủa Al(OH)3 đã sử dụng 0,2 mol H2SO4
n A l ( O H ) 3 = 0 , 4 m o l → n B a C O 3 = 0 , 25 = n B a ( O H ) 2 → n N a O H = 0 , 3 m o l
Bảo toàn nguyên tố trong X chứa 0,25 mol Ba, 0,4 mol Al và 0,7 mol Na
Bảo toàn e:
n O = 0 , 25 . 2 + 0 , 4 . 3 + 0 , 7 - 0 , 45 . 2 2 = 0 , 75 → m = 73 , 15 g a m

Đáp án C
Hòa tan hoàn toàn m gam X thu được dung dịch Y và 0,45 mol H2.
Do đồ thị như vậy nên giai đoạn đầu kết tủa tăng là do H2SO4 tác dụng với Ba(OH)2 tạo kết tủa BaSO4.
Giai đoạn kết tủa không đổi tiếp theo là H2SO4 trung hòa NaOH.
Giai đoạn kết tủa tăng lên do H2SO4 tác dụng với NaAlO2 tạo kết tủa Al(OH)3.
Giai đoạn kết tủa giảm do H2SO4 hòa tan Al(OH)3.
Giai đoạn kết tủa không đổi lúc này chỉ còn BaSO4
![]()
Kết tủa tối đa là 89,45 gam gồm Al(OH)3 và BaSO4.
Lúc đạt 0,75 mol H2SO4 kết tủa bị giảm đi 7,8 gam tương đương với 0,1 mol Al(OH)3.
Lúc này lượng H2SO4 cần để hòa tan là 0,15 mol.
Vậy lúc kết tủa đạt cực đại thì lượng H2SO4 đã dùng là 0,6 mol
Trong giai đoạn tạo kết tủa Al(OH)3 đã sử dụng 0,2 mol H2SO4
nNaOH = 0,3 mol
Bảo toàn nguyên tố trong X chứa 0,25 mol Ba, 0,4 mol Al và 0,7 mol Na
Bảo toàn e:
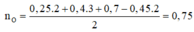
m = 73,15 gam

Đáp án A
+ Từ giả thiết suy ra X chứa MgSO 4 , FeSO 4 , Fe 2 ( SO 4 ) 3 Al 2 ( SO 4 ) 3 , ZnSO 4 , K 2 SO 4 + n KNO 3 = x ; n H 2 SO 4 = 2 x ⇒ m muối / X = 8 , 6 + 39 x + 2 x . 96 = 43 , 25 ⇒ x = 0 , 15 . + n H 2 = y ⇒ m Y = 50 y , n H 2 O = 0 , 3 - y . + BTKL : m kim loại + m ( KNO 3 , H 2 SO 4 ) = m muối + m Y + m H 2 O BTKL : m kim loại + m dd ( KNO 3 , H 2 SO 4 ) = m dd X + m Y ⇒ 8 , 6 + 0 , 15 . 101 + 0 , 3 . 98 = 43 , 25 + 50 y + 18 ( 0 , 3 - y ) 8 , 6 + 100 = m dd X + 50 y ⇒ y = 0 , 140625 m dd X = 101 , 56875 + KOH + X → dd chỉ chứa K 2 SO 4 + Z ↓ ⇒ n KOH = 2 n K 2 SO 4 - n KNO 3 = 0 , 45 n OH - trong Z = n KOH = 0 , 45 + Khi nung Z sẽ xảy ra quá trình : 0 , 45 mol OH - → 0 , 225 mol O 2 - O 2 → oxi hóa Fe 2 + z mol O 2 - ⇒ 0 , 225 . 16 + 16 z = 12 , 6 - 8 , 6 ⇒ z = 0 , 025 ⇒ BTE : n Fe 2 + = 2 n O 2 - = 0 , 05 ⇒ C % FeSO 4 = 152 . 0 , 05 101 , 56875 . 100 % = 7 , 48 % gần nhất với 7 , 5 %






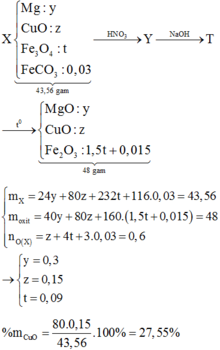


Định hướng tư duy
Dung dịch Y chứa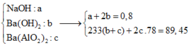
Tại vị trí 0,75 mol axit → A l 3 + : 0 , 1 N a + : a S O 4 2 - : 0 , 75 - ( b + c ) → a + 0 , 3 = 1 , 5 - 2 b - 2 c → a = 0 , 7 b = 0 , 05 c = 0 , 2
Chuyển dịch điện tích => m= 80,35-0,45.16= 73,15 => %O= 16,4%