Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.

\(R+H_2SO_4\rightarrow RSO_4+H_2\\ n_{H_2}=\dfrac{7,168}{22,4}=0,32\left(mol\right)\\ n_R=n_{H_2}=0,32\left(mol\right)\\ M_R=\dfrac{7,68}{0,32}=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow R\left(II\right):Magie\left(Mg=24\right)\)

- Cho 4,95 (g) R pư với HCl, thấy kim loại dư.
Ta có: \(n_{HCl}=\dfrac{5,475}{36,5}=0,15\left(mol\right)\)
PT: \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_{R\left(pư\right)}=\dfrac{1}{2}n_{HCl}=0,075\left(mol\right)\)
\(n_{R\left(banđau\right)}>0,075\Rightarrow\dfrac{4,95}{M_R}>0,075\Rightarrow M_R< 66\left(g/mol\right)\) (1)
- Cho 18,6 (g) hh Fe và R pư với H2SO4 dư.
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(R+H_2SO_4\rightarrow RSO_4+H_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{hh}=n_{Fe}+n_R=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow\overline{M_{hh}}=\dfrac{18,6}{0,3}=62\left(g/mol\right)\)
Mà: MFe < 62 (g/mol) → MR > 62 (g/mol) (2)
Từ (1) và (2) ⇒ 62 < MR < 66
→ R là Zn (65 g/mol)

a) \(n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
=> nHCl = 0,27 (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 5,85 + 0,27.36,5 - 0,135.2 = 15,435 (g)
b) VH2 = 3,024 (l) (Theo đề bài)
c)
Hỗn hợp kim loại gồm \(\left\{{}\begin{matrix}Al:a\left(mol\right)\\X:3a\left(mol\right)\end{matrix}\right.\)
=> 27a + MX.3a = 5,85
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
a----------------------->1,5a
X + 2HCl --> XCl2 + H2
3a------------------->3a
=> 1,5a + 3a = 0,135
=> a = 0,03 (mol)
=> MX = 56 (g/mol)
=> X là Fe

a) \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,5}{n}\left(mol\right)\)
Ta có : \(M_M=\dfrac{16,25}{\dfrac{0,5}{n}}=32,5n\)
Chạy nghiệm n
n=1 => M=32,5 (loại)
n=2 => M=65 ( chọn)
n=3 => M=97,5 (loại)
Vậy M là Zn
b) Ta có : \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(lít\right)\)

\(n_R=\dfrac{13}{M_R}\left(mol\right)\)
PTHH: R + H2SO4 --> RSO4 + H2
____\(\dfrac{13}{M_R}\)------------->\(\dfrac{13}{M_R}\)-->\(\dfrac{13}{M_R}\)
=> \(\dfrac{13}{M_R}\left(M_R+96\right)=32,2\)
=> MR = 65(g/mol)
=> R là Zn
\(n_{H_2}=\dfrac{13}{65}=0,2\left(mol\right)\)
=> VH2 = 0,2.22,4 = 4,48(l)
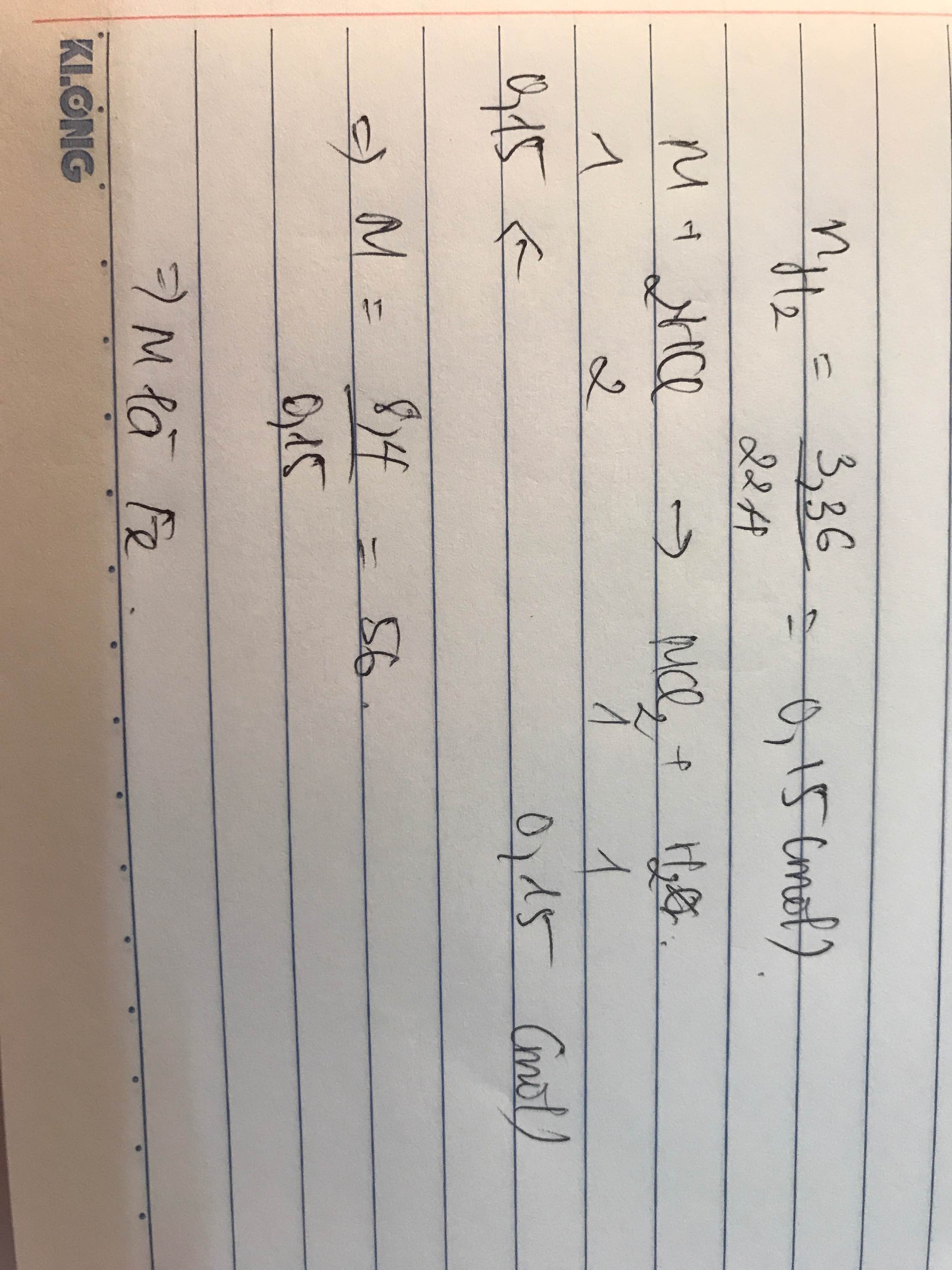
nH2 = 0,3 mol
R + 2HCl \(\rightarrow\) RCl2 + H2
nR = \(\dfrac{7,2}{R}\) = 0,3
\(\Rightarrow\) R = \(\dfrac{7,2}{0,3}\)= 24 ( Mg )
Vậy kim loại R là magie
nH2 = 6,72/22,4 = 0,3 mol
R +2HCl -> RCl2 + H2
0,3 <- 0,3 <- 0,3 <- 0,3 mol
MR= m/n = 7,2/0,3 = 24
vậy R là Mg