Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng

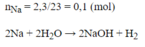
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Hoà tan hết 2,3g Na kim loại vào 97,8g nước . Hãy tính nồng độ % của dung dịch thu được sau phản ứng

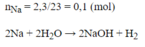


C % N a O H = m N a O H m dd .100 % = 0,1.40 100 .100 % = 4 % .
Đáp án B

Sửa lại :
nNa=0,1
2Na+2H2O-->2NaOH+H2
0,1-----------------0,1-------0,05
=>Cm NaOH=0,1/0,0978=1,02M
mNaOH=4g
=>C% NaOH=4*100/(2,3+97,8-0,05*2)=4%

mik sửa lại cái dưới bị lỗi latex
\(a.n_{HCl}=0,05.2=0,1\left(mol\right);n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.C_{M_{AlCl_3}}=\dfrac{0,3.2:3}{0,05}=0,4M\\ C_{M_{HCl\left(dư\right)}}=\dfrac{0,1-\left(0,3.6:3\right)}{0,05}=0,8M\)
\(a.n_{HCl}=0,05.2=0,1\left(mol\right)\\ n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\ 2R+6HCl\rightarrow2RCl_3+3H_2\\ \Rightarrow\dfrac{0,1}{6}>\dfrac{0,03}{3}\Rightarrow HCl.dư,R.pư.hết\\ n_R=0,03.2:3=0,02\left(mol\right)\\ M_R=\dfrac{0,54}{0,02}=27\left(g/mol\right)\\ \Rightarrow R=27\left(Al,nhôm\right)\\ b.n_{AlCl_3}=n_{Al}=0,02mol\\ C_{M_{AlCl_3}}=\dfrac{0,02}{0,05}=0,4M\\ C_M_{HCl\left(dư\right)}=\dfrac{0,1-\left(0,03.2\right)}{0,05}=0,8M\)

a,\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: x 0,5x
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}23x+137y=36,6\\0,5x+y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,4\\y=0,2\end{matrix}\right.\)
\(\%m_{Na}=\dfrac{0,4.23.100\%}{36,6}=25,17\%;\%m_{Ba}=100-25,17=74,83\%\)
b,
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,4 0,4
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Mol: 0,2 0,2
mdd sau pứ = 36,6+167,2-0,4.2 = 203 (g)
\(C\%_{ddNaOH}=\dfrac{0,4.40.100\%}{203}=7,88\%\)
\(C\%_{ddBa\left(OH\right)_2}=\dfrac{0,2.171.100\%}{203}=16,85\%\)

\(n_{Na_2O}=\dfrac{15,5}{62}=0,25\left(mol\right)\\ PTHH:Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=2.0,25=0,5\left(mol\right)\\ a,C_{MddNaOH}=\dfrac{0,5}{0,5}=1\left(M\right)\\ b,2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ n_{H_2SO_4}=n_{Na_2SO_4}=\dfrac{0,5}{2}=0,25\left(mol\right)\\ m_{H_2SO_4}=0,25.98=24,5\left(g\right)\\ m_{ddH_2SO_4}=\dfrac{24,5.100}{20}=122,5\left(g\right)\\ V_{ddH_2SO_4}=\dfrac{122,5}{1,14}\approx107,456\left(ml\right)\\ c,V_{ddsau}=V_{ddNaOH}+V_{ddH_2SO_4}\approx0,5+0,107456=0,607456\left(l\right)\\C_{MddNa_2SO_4}\approx\dfrac{ 0,25}{0,607456}\approx0,411552\left(M\right)\)

\(n_{H_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
____0,35_____0,7___________0,35 (mol)
a, \(m_{Zn}=0,35.65=22,75\left(g\right)\)
b, \(C\%_{HCl}=\dfrac{0,7.36,5}{200}.100\%=12,775\%\)

200ml dung dịch H2SO4 loãng.
a) Cu không phản ứng với H2SO4 loãng.
Zn + H2SO4 --> ZnSO4 + H2
b) nH2 = \(\dfrac{1,12}{22,4}\)=0,05 mol => nZn = 0,05 mol
mZn = 0,05.65 = 3,25 gam <=> mCu = 8,5 - 3,25 = 5,25 gam
Chất rắn thu được sau phản ứng chính là Cu không phản ứng = 5,25 gam.
c)
nH2SO4 = nH2 = 0,05 mol
=> CH2SO4 = \(\dfrac{n}{V}\)= \(\dfrac{0,05}{0,2}\)= 0,25 M

\(a,PTHH:2Na+2H_2O\rightarrow2NaOH+H_2\\ n_{Na}=\dfrac{2,3}{23}=0,1mol\\ n_{NaOH}=0,1.2=0,2mol\\ C_{M_{NaOH}}=\dfrac{0,2}{0,5}=0,4M\\ b,oxit.kl:RO\\ n_{RO}=\dfrac{2,4}{R+16}mol\\ n_{HCl}=\dfrac{30.7,3}{100.36,5}=0,06mol\\ RO+2HCl\rightarrow RCl_2+H_2O\\ \Rightarrow\dfrac{2,4}{R+16}=0,06:2\\ \Leftrightarrow R=64,Cu\)