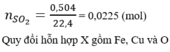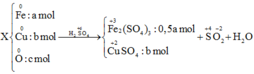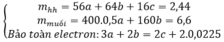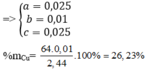Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

![]()
![]()
![]()
![]()
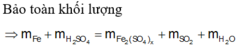
=> 8,4+0,4.98=0,075(56.2+96x)+(0,4-0,075x).64+0,4.18
=> x=8/3
m_muối=0,075(56.2+96.8/3)=27,6 gam
![]()

Coi hỗn hợp X gồm : Fe , O
\(n_{Fe}=a\left(mol\right),n_O=b\left(mol\right)\)
\(m_X=56a+16b=30\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
\(\text{Bảo toàn e : }\)
\(3n_{Fe}=2n_O+2n_{SO_2}\)
\(\Rightarrow3a=2b+1\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.475,b=0.2125\)
\(n_{Fe_2\left(SO_4\right)_3}=\dfrac{0.475}{2}=0.2375\left(mol\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0.2375\cdot400=95\left(g\right)\)
Coi X gồm Fe(a mol) ; O(b mol)
=> 56a + 16b = 30(1)
n SO2 = 11,2/22,4 = 0,5(mol)
Bảo toàn e : 3n Fe = 2n O + 2n SO2
<=> 3a - 2b = 1(2)
Từ (1)(2) suy ra a = 0,475 ; b = 0,2125
n Fe2(SO4)3 = 0,5a = 0,2375(mol)
=> m = 0,2375.400 = 95(gam)
Thí nghiệm 2 :
Gọi n FeSO4 = y(mol) ; n Fe2(SO4)3 = x(mol)
Bảo toàn nguyên tố Fe : x + y = 0,475
Bảo toàn e : 2x.3 + 2y = 0,2125.2
=> x = -0,13125 <0
(Sai đề)

$n_{SO_2} = 0,01(mol)$
Bảo toàn nguyên tố với S :
$n_{H_2SO_4} = 3n_{Fe_2(SO_4)_3} + n_{SO_2}$
$\Rightarrow n_{Fe_2(SO_4)_3} = \dfrac{0,1 - 0,01}{3} = 0,03(mol)$
$z = 0,03.400 = 12(gam)$
$n_{Fe} = 2n_{Fe_2(SO_4)_3} = 0,06(mol)$
Bảo toàn e : $3n_{Fe} = 2n_O + 2n_{SO_2} \Rightarrow n_O = \dfrac{0,06.3 - 0,01.2}{2} = 0,08(mol)$
$n_{Fe} : n_O = 0,06 : 0,08 = 3 : 4$
Vậy oxit là $Fe_3O_4$
$m + z = \dfrac{0,06}{3}.232 + 12 = 16,64$

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=0,2.1,5=0,3\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\) => Mg hết, H2SO4 dư
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,2-->0,2------>0,2----->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
\(\left\{{}\begin{matrix}C_{M\left(MgSO_4\right)}=\dfrac{0,2}{0,2}=1M\\C_{M\left(H_2SO_4.dư\right)}=\dfrac{0,3-0,2}{0,2}=0,5M\end{matrix}\right.\)

\(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe}=5,6\left(g\right)\)
\(\Rightarrow m_{Fe_2O_3}=16\left(g\right)\)
\(\Rightarrow n_{Fe}=2n_{Fe_2O_3}=0,2\left(mol\right)=n_{FeCl_3}\)
Lại có : \(n_{HCl}=2n_{H_2}+3n_{FeCl_3}=0,8\left(mol\right)\)
\(\Rightarrow m_{ddHCl}=292\left(g\right)\)
\(\Rightarrow V=\dfrac{2920}{11}\left(ml\right)=\dfrac{73}{275}\left(l\right)\)
\(\Rightarrow C_{MFeCl_3}=\dfrac{0,2}{\dfrac{73}{275}}=\dfrac{55}{73}\left(M\right)\)

a)
Gọi số mol Fe, Al là a, b (mol)
=> 56a + 27b = 19,3 (1)
\(n_{H_2}=\dfrac{14,56}{22,4}=0,65\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a--->a---------------->a
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b---->1,5b------------------->1,5b
=> a + 1,5b = 0,65 (2)
(1)(2) => a = 0,2 (mol); b = 0,3 (mol)
mFe = 0,2.56 = 11,2 (g); mAl = 0,3.27 = 8,1 (g)
b)
\(n_{H_2SO_4}=0,65\left(mol\right)\)
=> \(C_{M\left(dd.H_2SO_4\right)}=\dfrac{0,65}{0,2}=3,25M\)