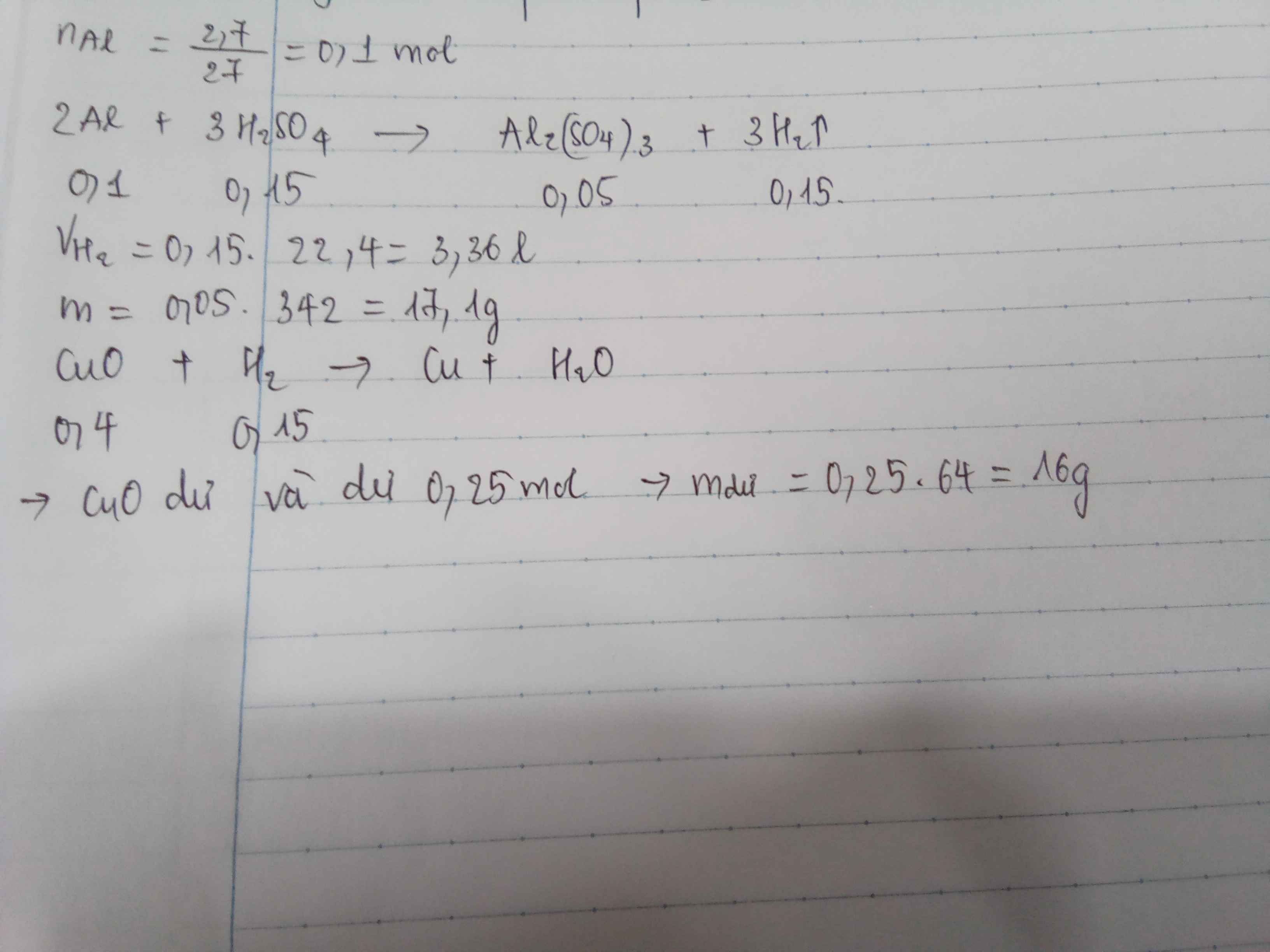Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
b) nH2 =\(\dfrac{26,88}{22,4}\)=1,2 mol
Theo tỉ lệ phản ứng => nAl phản ứng = \(\dfrac{nH_2.2}{3}\)= 0,8 mol
=> mAl phản ứng = 0,8.27= 21,6 gam
c) nAl2(SO4)3 = 1/2 nAl = 0,4 mol
=> m Al2(SO4)3 = 0,4. 342 = 136,8 gam
a) 2Al+3H2SO4⟶Al2(SO4)3+3H2↑2Al+3H2SO4⟶Al2(SO4)3+3H2↑
b) mAl=21,6gmAl=21,6g
c) mAl2(SO4)3=136,8gmAl2(SO4)3=136,8g
Giải thích các bước giải:
a) Phương trình hoá học:
2Al+3H2SO4⟶Al2(SO4)3+3H2↑2Al+3H2SO4⟶Al2(SO4)3+3H2↑
b) Số mol H2H2 sinh ra sau phản ứng:
nH2=VH222,4=26,8822,4=1,2molnH2=VH222,4=26,8822,4=1,2mol
Dựa vào phương trình hóa học ta được:
nAl=23nH2=23⋅1,2=0,8molnAl=23nH2=23⋅1,2=0,8mol
Khối lượng AlAl tham gia phản ứng:
mAl=nAl.MAl=0,8.27=21,6gmAl=nAl.MAl=0,8.27=21,6g
c) Dựa vào phương trình hóa học ta được:
nAl2(SO4)3=13nH2=13⋅1,2=0,4molnAl2(SO4)3=13nH2=13⋅1,2=0,4mol
Khối lượng muối tạo thành:
mAl2(SO4)3=nAl2(SO4)3.MAl2(SO4)3=0,4.342=136,8gmAl2(SO4)3=nAl2(SO4)3.MAl2(SO4)3=0,4.342=136,8g

a) CaCO3 + 2HCl → CaCl2 + H2O + CO2
b) nCaCO3 = \(\dfrac{450}{100}\)=4,5 mol
=> nHCl phản ứng = 4,5.2 = 9mol
<=> mHCl = 9 . 36,5 = 328,5 gam
c) nCO2 = nCaCO3 = 4,5 mol => V CO2 = 4,5 . 22,4 = 100,8 lít

Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a. PTHH:
\(Mg+2HCl--->MgCl_2+H_2\left(1\right)\)
\(MgO+2HCl--->MgCl_2+H_2O\left(2\right)\)
b. Theo PT(1): \(n_{Mg}=n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,2.24=4,8\left(g\right)\)
\(\Rightarrow m_{MgO}=8-4,8=3,2\left(g\right)\)
c. Ta có: \(n_{hh}=0,2+\dfrac{3,2}{40}=0,28\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_{hh}=2.0,28=0,56\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,56.36,5=20,44\left(g\right)\)

\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right);n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(PTHH:2Mg+O_2-^{t^o}\rightarrow2MgO\) (1)
Theo đề : 0,3........0,1
Lập tỉ lệ: \(\dfrac{0,3}{2}>\dfrac{0,1}{1}\) => Mg dư, O2 phản ứng hết
\(n_{Mg\left(pứ\right)}=2n_{O_2}=0,2\left(mol\right)\)
\(Mg_{dư}+2HCl\rightarrow MgCl_2+H_2\uparrow\)(2)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\) (3)
Khí Y là H2
Theo PT (2) : \(n_{H_2}=n_{Mg\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Dung dịch X là MgCl2
\(m_{ddsaupu}=0,1.24+0,2.40+75-0,1.2=85,2\left(g\right)\)
=>\(C\%_{MgCl_2}=\dfrac{\left(0,2+0,1\right).95}{85,2}.100=33,45\%\)

2) n Mg = \(\dfrac{7,2}{24}\) = 0,3 (mol)
n O2 = \(\dfrac{2,24}{22,4}\)= 0,1 (mol)
Mg + 1/2O2 --to> MgO
0,2 <--- 0,1 --------> 0,2
n Mg dư = 0,3 - 0,2 = 0,1 (mol)
n MgO = 0,2 (mol)
MgO + 2HCl --> MgCl2 + H2O
0,2 ------> 0,4 (mol)
Mg + 2HCl --> MgCl2 + H2
0,1 --> 0,2 ------- --------> 0,1 (mol)
V H2 = 0,1 . 22,4 = 2,24 (lít)
m Ct=\(\dfrac{100.29,2\%}{100\%}\)=92,2g
m HCl = \(\dfrac{29,2}{36,5}\) = 0,8 (mol) > 0,6 (mol) Pứ hết cho ra MgCl2
m dd = m MgO + m Mg + m HCl dd - m H2
= 0,2.40 + 0,1.24 + 100 - 0,1.2 = 110,2 (g)
\(C\%=\dfrac{0,3.95}{110,2}.100\%=25,86\%\)
2) n Mg = \(\dfrac{7,2}{24}\) = 0,3 (mol)
n O2 = \(\dfrac{2,24}{22,4}\)= 0,1 (mol)
Mg + 1/2O2 --to> MgO
0,2 <--- 0,1 --------> 0,2
n Mg dư = 0,3 - 0,2 = 0,1 (mol)
n MgO = 0,2 (mol)
MgO + 2HCl --> MgCl2 + H2O
0,2 ------> 0,4 (mol)
Mg + 2HCl --> MgCl2 + H2
0,1 --> 0,2 ------- --------> 0,1 (mol)
V H2 = 0,1 . 22,4 = 2,24 (lít)
m Ct=\(\dfrac{100.29,2\%}{100\%}\)
m HCl = \(\dfrac{29,2}{36,5}\) = 0,8 (mol) > 0,6 (mol) Pứ hết cho ra MgCl2
m dd = m MgO + m Mg + m HCl dd - m H2
= 0,2.40 + 0,1.24 + 100 - 0,1.2 = 110,2 (g)
\(C\%=\dfrac{0,3.95}{110,2}.100\%=25,86\%\)

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 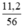 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 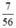 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 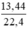 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

\(PTHH:4Al+3O_2->2Al_2O_3\)
BĐ 0,4 0,27 (mol)
PU 0,36---->0,27---->0,18 (mol)
CL 0,04---->0------>0,18 (mol)
b)
\(n_{Al}=\dfrac{m}{M}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{6,048}{22,4}=0,27\left(mol\right)\)
\(\dfrac{n_{Al}}{4}>\dfrac{n_{O_2}}{3}\left(\dfrac{0,4}{4}>\dfrac{0,27}{3}\right)\)
=> Al dư, O2 hết (tính theo O2)
\(m_{Al}=n\cdot M=0,04\cdot27=1,08\left(g\right)\)
c)
\(m_{Al_2O_3}=n\cdot M=0,18\cdot\left(27\cdot2+16\cdot3\right)=18,36\left(g\right)\)
a, PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Ta có: \(n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{6,048}{22,4}=0,27\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,4}{4}>\dfrac{0,27}{3}\), ta được Al dư.
Theo PT: \(n_{Al\left(pư\right)}=\dfrac{4}{3}n_{O_2}=0,36\left(mol\right)\)
\(\Rightarrow n_{Al\left(dư\right)}=0,4-0,36=0,04\left(mol\right)\)
\(\Rightarrow m_{Al\left(dư\right)}=0,04.27=1,08\left(g\right)\)
c, Theo PT: \(n_{Al_2O_3}=\dfrac{2}{3}n_{Al}=0,18\left(mol\right)\)
\(\Rightarrow m_{Al_2O_3}=0,18.102=18,36\left(g\right)\)

Mình thay trên câu a luôn nhé.
5. Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
a) Ta có PTHH :
Fe + 2HCl \(\rightarrow\) FeCl2 + H2\(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,1 mol 0,2 mol 0,1 mol 0,1 mol
Số mol của Fe là :
nFe = 5,6/56 = 0,1 (mol)
b) Khối lượng của FeCl2 tạo thành sau p.ứng là :
mFeCl2 = 0,1.127 = 12,7 (g)
c) Thể tích khí Hiđro (đktc) tạo thành sau p.ứng là :
VH2 = 0,1.22,4 = 2,24 (l)
4. Công thức của B là : NaxCyOz
+ \(m_{Na}=\frac{106.43,6}{100}\approx46\left(g\right)\)
\(m_C=\frac{106.11,3}{100}\approx12\left(g\right)\)
\(m_O=\frac{106.45,3}{100}\approx48\left(g\right)\)
+ \(n_{Na}=\frac{46}{23}=2\left(mol\right)\)
\(n_C=\frac{12}{12}=1\left(mol\right)\)
\(n_O=\frac{48}{16}=3\left(mol\right)\)
Suy ra trong một p.tử h/c có 2 n.tử Na, 1 n.tử C và 3 n.tử O.
\(\Rightarrow\) CTHH của hợp chất B là Na2CO3.