Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
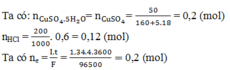
Thứ tự điện phân tại catot và anot là:
Tại catot: Cu2+ + 2e → Cu
0,1 0,2 0,1
⟹ Cu2+ chưa bị điện phân hết.
⟹ mkim loại ở catot = 0,1.64 = 6,4 (gam)
Tại anot: 2Cl– → Cl2 + 2e
0,12 0,06 0,12
⟹ ne (do Cl– nhường) = 0,12 < 0,2 mol
⟹ tại anot Cl– đã bị điện phân hết và đến nước bị điện phân.
Ta có: ne (do H2O nhường) = 0,2 – 0,12 = 0,08 (mol)
2H2O → O2 + 4H + 4e
0,02 ⟵ 0,08
Vkhí thoát ra ở anot = (0,06 + 0,02).22,4 = 1,792 (lít).

Chọn A.
Tại thời điểm t (s) tại anot thu được khí Cl2 (0,05 mol) Þ ne (1) = 0,1 mol
Tại thời điểm 3,5t (s) tại anot có:
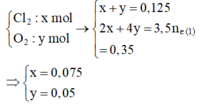
![]() và dung dịch Y chứa Cu2+ dư (a mol), H+ (0,2 mol), NO3-, K+
và dung dịch Y chứa Cu2+ dư (a mol), H+ (0,2 mol), NO3-, K+
Khi cho Y tác dụng với Fe thì: nFe pư =
= 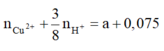
Chất rắn thu được gồm Fe dư và Cu Þ 20 – 56.(a + 0,075) + 64a = 16,4 Þ a = 0,075
Vậy dung dịch X gồm Cu(NO3)2 (0,25 mol) và KCl (0,15 mol) Þ m = 58,175 (g).

Chọn C.
Dung dịch Y chứa H+ với n H + = 2 n H 2 = 0 , 12 mol ⇒ H + ban đầu: 0 , 12 + 2 n H 2 ⇒ n O 2 = 0 , 03 + 0 , 5 n H 2
Khối lượng dung dịch giảm:
m Cu + m khí = 300 - 283 , 32 = 16 , 68 ⇒ 64 n Cu + 71 n Cl 2 + 18 n H 2 = 15 , 72 (1)
→ BT : e 2 n Cu = 0 , 12 + 2 n Cl 2 (2) và
160 n Cu + 117 n Cl 2 = 31 , 76 (3)
Từ (1), (2), (3) suy ra:
n Cu = 0 , 14 mol ; n Cl 2 = 0 , 08 mol ; n H 2 = 0 , 06 mol ⇒ n O 2 = 0 , 06 mol
Vậy V = 3,136 lít.
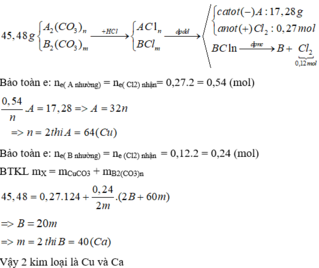


Đáp án A