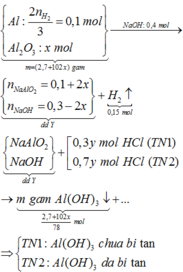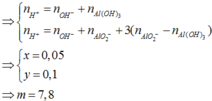Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nNaOH ban đầu = 0,4 mol
Al + NaOH ⟶ NaAlO2 + 3/2H2
0,1 0,1 0,15
![]()
Al2O3 + 2NaOH⟶2NaAlO2 + H2O
a 2a
(dư 0,3-2a)
⟶ m = 2,7 + 102a.
Lập hệ phương trình →a = 0.05 → m = 7,8
Đáp án B

Đáp án D
Số mol HCl dư =0,1 (mol)
Số mol kết tủa
![]()
Số mol ![]()
Số mol HCl ban đầu = 3 . 0 , 1 + 0 , 1 = 0 , 4 ⇒ a = 2

Giải thích:
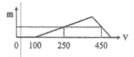
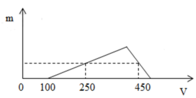
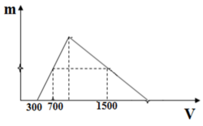
Ta chia đồ thị làm 3 giai đoạn
Giai đoạn 1: bắt đầu xuất hiện kết tủa => hết VNaOH = 100 ml => đây là lượng thể tích cần dùng để trung hòa lượng HCl còn dư sau phản ứng
=> nHCl dư = 0,1 (mol)
Giai đoạn 2: đồ thi bắt đầu đi lên đến điểm cực đại
Tại giai đoạn này xảy ra phản ứng:
Al3+ + 3OH- → Al(OH)3↓
(0,25 – 0, 1) → 0,05 (mol)
Giai đoạn 3: đồ thị đi xuống, tại giai đoạn này lượng kết tủa bị hòa tan theo phản ứng
Al(OH)3 + OH- → AlO2− + 2H2O
Từ đồ thị ta thấy tại giá trị VNaOH = 250 ml và VNaOH = 450 ml cùng thu được một lượng kết tủa như nhau
=> áp dụng công thức nhanh ta có:
nNaOH = 4nAl3+ - nAl(OH)3 + nH+ dư
=> 0,45 = 4a – 0,05 + 0,1
=> a = 0,1 (mol)
Vậy để lượng kết tủa cực đại thì tất cả lượng Al3+ sẽ chuyển hết thành Al(OH)3
=> nAl(OH)3 = nAl3+ = 0,1 (mol) => mAl(OH)3 = 0,1.78 = 7,8(g)
Đáp án D

Đáp án B
Ta có:
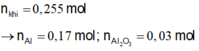
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
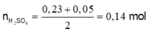
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3 m o l
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng


Đáp án B
Ta có: n k h i = 0 , 255 m o l
![]()
Dung dịch Y chứa 0,23 mol AlCl3.
Cho dung dịch chứa 0,3 mol Ba(OH)2 và 0,37 mol NaOH tác dụng với Y thu được dung dịch Z.
Z chứa Ba2+ 0,3 mol, Na+ 0,37 mol, AlO2- 0,23 mol, OH- dư 0,05 mol.
Cho H2SO4 vào Z.
Để kết tủa Al(OH)3 lớn nhất thì :
n H 2 S O 4 = 0 , 23 + 0 , 05 2 = 0 , 14 m o l
Để kết tủa BaSO4 lớn nhất thì : n H 2 S O 4 = 0 , 3
Lúc kết tủa BaSO4 tối đa thì Al(OH)3 bị hòa tan nhưng lượng BaSO4tạo thành lớn hơn Al(OH)3 bị hòa tan nên kết tủa vẫn tăng
→ V = 0 , 3 2 = 150 m l

Đáp án D
Theo giả thiết, ta có :

Quy đổi hỗn hợp X thành Fe và O. Theo bảo toàn khối lượng, bảo toàn electron, bảo toàn điện tích cho dung dịch Z và bảo toàn nguyên tố N, Fe, ta có :
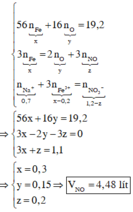

Giải thích:
2Na + 2H2O → 2NaOH + H2
2NaOH + Al2O3 → 2 NaAlO2 + H2O
Y dư NaOH
Thì HCl + NaOH → NaCl + H2O
HCl + NaAlO2 +H2O → NaCl + Al(OH)3
3HCl + Al(OH)3 → AlCl3 + 3H2O
Y có nNaOH = 0,3 mol và nNaAlO2 = a mol
Khi thêm 700 ml dung dịch HCl vào thì n↓ = 0,7 - 0,3 = 0,4 mol
Khi thêm 1500 ml dung dịch HCl vào thì n↓= a – (1,5 – 0,3 –a ): 3
→ a – (1,5 – a – 0,3) : 3 = 0,4 (mol) → a = 0,6 mol
→ bảo toàn Na có nNa = a + 0,3 = 0,9 mol → nH2 = 0,45 mol → x =0,45 . 22,4 = 10,08
Đáp án D