Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a)2Al+HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
b) \(n_{HCl}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\ Gọi:n_{Al}=x\left(mol\right);n_{Fe}=y\left(mol\right)\\ Tacó:\left\{{}\begin{matrix}27x+56y=m_{hh}\\\dfrac{3}{2}x+y=0,4\end{matrix}\right.\)
Đề thiếu dữ kiện, xem lại đề nha bạn !

a, Ta có: 27nAl + 56nFe = 22 (1)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{19,832}{24,79}=0,8\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4\left(mol\right)\\n_{Fe}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,4.27}{22}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)
b, \(n_{HCl}=2n_{H_2}=1,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{1,6}{0,5}=3,2\left(M\right)\)

a, Ta có: 27nAl + 56nFe = 27,8 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{17,353}{24,79}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{27,8}.100\%\approx19,42\%\\\%m_{Fe}\approx80,58\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=n_{H_2}=0,7\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,7}{0,5}=1,4\left(M\right)\)

a,\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: x x
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: y 1,5y
Ta có: \(\left\{{}\begin{matrix}24x+27y=12,6\\x+1,5y=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
b,\(\%m_{Mg}=\dfrac{0,3.24.100\%}{12,6}=57,14\%;\%m_{Al}=100-57,14=42,86\%\)
c,
PTHH: Mg + H2SO4 → MgSO4 + H2
Mol: 0,3 0,3 0,3
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,2 0,3 0,1
\(C_{M_{ddH_2SO_4}}=\dfrac{0,3+0,3}{0,5}=1,2M\)
\(C_{M_{ddMgSO_4}}=\dfrac{0,3}{0,5}=0,6M;C_{M_{ddAl_2\left(SO_4\right)_3}}=\dfrac{0,1}{0,5}=0,2M\)



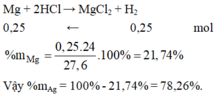
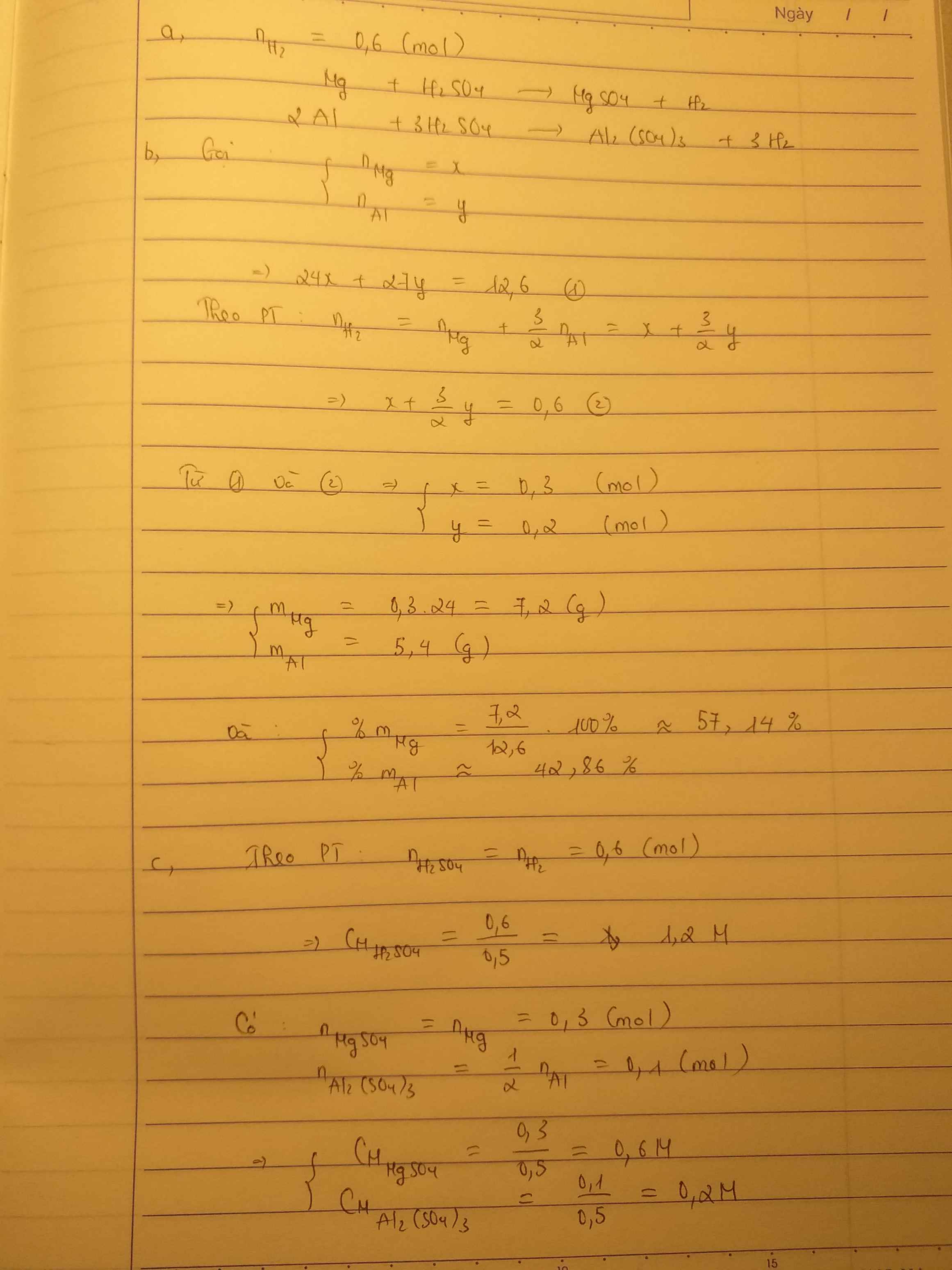
PTHH:
Fe + 2HCl -> FeCl2 + H2
b b
Mg + 2HCl -> MgCl2 + H2
a a
=> Ta có: 24a + 56a = 3,68 ; ( a + b ) x 22,4 = 2,24
=> a = 0,06 b = 0,04
Khối lượng của Mg có trong hỗn hợp là: m = M . n = 0,06 x 24 = 1,14 ( g )
Thành phần phần trăm theo khối lượng của Mg trong hỗn hợp là: 1,14 x 100 / 3,68= 39,1 %
Thành phần phần trăm theo khối lượng của Fe trong hỗn hợp là: 100% - 39,1% = 60,9%