Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án C
Tại anot, trong t giây thu được nO2 = 0,035
=> Trong 2t giây thu được nO2 = 0,07
=> nH2 = 0,1245 - 0,07 = 0,0545 mol
Bảo toàn electron trong 2t giây:
2nM + 2nH2 = 4nO2 => nM = 0,0855
=>M+ 96 = 13,68/0,0855
=> M = 64: Cu
Bảo toàn electron trong t giây:
2nCu = 4nO2 => nCu = 0,07 => mCu = y = 4,48

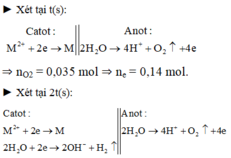
⇒ ne = 0,14 × 2 = 0,28 mol; nO2 = 0,035 × 2 = 0,07 mol < 0,1245 mol.
⇒ khí còn chứa H2 ⇒ M2+ ở catot bị điện phân hết ⇒ nH2 = 0,0545 mol.
⇒ nMSO4 = nM2+ = (0,28 - 0,0545 × 2) ÷ 2 = 0,0855 mol
⇒ MMSO4 = 13,68 ÷ 0,0855 = 160 ⇒ MM = 64 ⇒ M là Đồng (Cu).
► y = 0,14 ÷ 2 × 64 = 4,48(g)
Đáp án C

Đáp án C
Ta có n N a C l = 0 , 18 mol
Trong thời gian t giây ở anot thu được 0,15 mol khí trong đó có 0,09 mol Cl2 và còn lại là O2 0,06 mol.
→ n e = 0,09.2 + 0,06.4 = 0,42 mol
Khi thời gian điện phân là 2 t giây → n e = 0.84 mol
Vậy ở anot thu đươc 0,09 mol Cl2 và 0,165 mol O2.
Vậy ở catot thu được H2 0,17 mol.
Bảo toàn e:

= n M S O 4 . 5 H 2 O
Vậy M là Ni (59).
Tại thời gian t giây ta thu được ở catot là 0,21 mol Ni => m = 12,39 gam
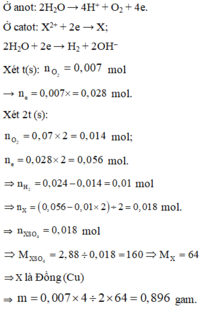


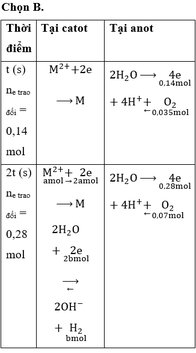


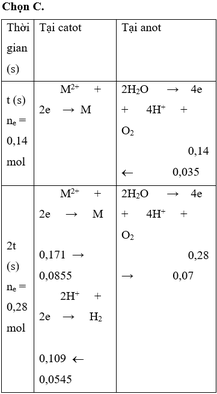
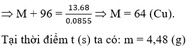
Đáp án C.
+ t giây: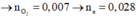
+ 2t giây: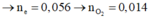
=> X = Cu