Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
cho 16g oxit sắt tác dụng với 120ml dd HCL thì thu được 32,5g muối khan. Tính nồng độ mol cua dd HCL

PTPƯ:
FexOy + 2yHCI -------------> xFeCI2y/x +yH2O
1mol ----------------------------> xmol
16/(56x +16y)mol-------------> 32,5/(56 + 71y/x)
=> 16x/(56x + 16y) = 32,5/(56 + 71y/x)
=> 896x +1136y = 1820x + 520y
=>616y = 924x
=> x/y = 2/3
Vậy CT của oxít sắt là Fe2O3
=>Fe2O3+3H2SO4->Fe2(SO4)3+3H2O
0,1---------------0,3
n Fe2O3=0,1 mol
=>CMHCl=\(\dfrac{0,3}{0,12}\)=2,5M

\(n_{Fe_xO_y}=\dfrac{16}{56x+16y}\left(mol\right)\)
PTHH: \(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)
\(\dfrac{16}{56x+16y}\)----------->\(\dfrac{16x}{56x+16y}\)
=> \(\dfrac{16x}{56x+16y}\left(56+35,5.\dfrac{2y}{x}\right)=32,5\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
0,1--->0,6
=> \(C_M=\dfrac{0,6}{0,12}=5M\)
à còn về câu "muối khan là gì" thì nó là muối không ngậm nước nhé

\(n_{Fe_xO_y}=\dfrac{32}{56x+16y}\left(mol\right)\)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{32}{56x+16y}\)----------->\(\dfrac{32x}{56x+16y}\)
=> \(\dfrac{32x}{56x+16y}=\dfrac{22,4}{56}=0,4\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHH: Fe2O3
\(n_{Fe}=\dfrac{22,4}{56}=0,4mol\)
\(Fe_xO_y+yH_2\rightarrow xFe+yH_2O\)
\(\dfrac{0,4}{x}\) 0,4
\(\Rightarrow M=\dfrac{32}{\dfrac{0,4}{x}}=80x\)
Mà \(M_{Fe_xO_y}=56x+16y=80x\Rightarrow16y=24x\Rightarrow\dfrac{x}{y}=\dfrac{16}{24}=\dfrac{2}{3}\)
\(\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\Rightarrow Fe_2O_3\)

a)\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH2O\)
Ta có: \(n_{FeCl_{\dfrac{2y}{x}}}=xn_{Fe_xO_y}=0,1x\left(mol\right)\)
\(\Rightarrow M_{FeCl_{\dfrac{2y}{x}}}=\dfrac{32,5}{0,1x}\)
| x | 1 | 2 | 3 |
| \(M_{FeCl_{\dfrac{2y}{x}}}\) | 325(loại) | 162,5(TM) | 108,33(loại) |
=> Muối có CT: \(FeCl_2\Rightarrow\)CT oxit là FeO
\(FeO+2HCl\rightarrow FeCl_2+H2O\)
0,1---->0,2(mol)
\(\Rightarrow V_{HCl}=\dfrac{0,2}{2}=0,1\left(l\right)\)
b) \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H2O\)
0,1<---------------0,2
\(\Rightarrow m_{Ba\left(OH\right)2}=0,1.171=17,1\left(g\right)\)
\(\Rightarrow m_{dd}=\dfrac{17,1.100}{17,1}=100\left(g\right)\)
Chúc bạn học tốt ^^

Vì sau phản ứng chỉ thu được 1 oxit sắt nên oxit sắt không phải là oxi sắt từ.
Gọi CT oxit là Fe2Oa
Fe2Oa(\(\dfrac{10,8}{112+16a}\))+2aHCl→2FeCla(\(\dfrac{10,8}{56+8a}\))+aH2O
nFe2Oa=\(\dfrac{10,8}{112+16a}\)
⇒\(\dfrac{10,8}{56+8a}.\left(56+35,5a\right)=19,05\)
⇔a=2
Vậy CT của oxit sắt là FeO

Gọi công thức hóa học của oxit sắt là F e x O y
PTHH của phản ứng là:
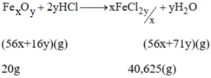
Theo PTHH ta có:
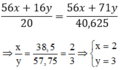
Vậy công thức hóa học của oxit sắt là F e 2 O 3

Bài 5 :
\(n_{HCl}=\dfrac{69,52\cdot1,05\cdot10}{100\cdot36,5}=0,2\left(mol\right)\) ; \(n_{Fe_xO_y}=\dfrac{7,2}{56x+16y}\left(mol\right)\)
PTHH : \(Fe_xO_y+2yHCl-->xFeCl_{\dfrac{2y}{x}}+yH_2O\)
Theo pthh : \(n_{Fe_2O_y}=\dfrac{n_{HCl}}{2y}=\dfrac{0,2}{2y}=\dfrac{0,1}{y}\left(mol\right)\)
=> \(\dfrac{7,2}{56x+16y}=\dfrac{0,1}{y}\)
=> \(x=y\)
=>CTHH của oxit sắt : \(FeO\)



PTPƯ:
FexOy + 2yHCI -------------> xFeCI2y/x +yH2O
1mol ----------------------------> xmol
16/(56x +16y)mol-------------> 32,5/(56 + 71y/x)
=> 16x/(56x + 16y) = 32,5/(56 + 71y/x)
=> 896x +1136y = 1820x + 520y
=>616y = 924x
=> x/y = 2/3
Vậy CT của oxít sắt là Fe2O3
16x ở đâu ra vậy ad