
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



b. - Trích mỗi chất một ít làm mẫu thử.
| Na2O | P2O5 | MgO | |
| Qùy tím ẩm | Hóa xanh | Hóa đỏ | Không đổi màu |
PTHH:
\(Na_2O+H_2O\rightarrow2NaOH\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\)
e.Dùng que diêm :
+Nếu cho diêm vào mà không có lửa thì đó là khí CO2
+Cho tàn đóm lửa của que diêm vào bình nếu bùng cháy là có khi Oxi
+Nếu như lửa trong bình khí đó cháy càng ngày càng to và bắt đầu chuyển sang màu xanh nhạt thì đó chính là khí Hidro


nH2=2,688/22,4=0,12(MOL)
pthh: Fe + 2 HCl -> FeCl2 + H2
0,12______0,24_____0,12____0,12(mol)
=>mFe=0,12.56=6,72(g)
%mFe=(6,72/8,72).100=77,064%
=>%mCu=22,936%

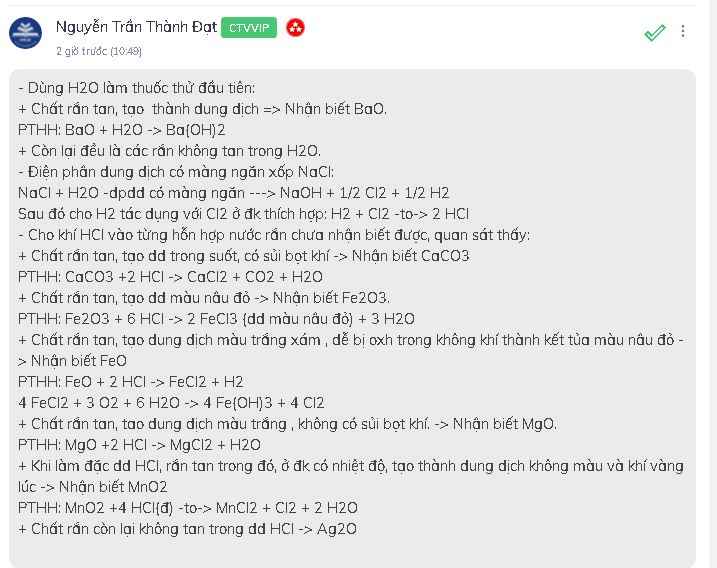
Trích mẫu thử
Cho mẫu thử vào dung dịch $HCl$
- mẫu thử tan, tạo khí là $Fe + FeO$ và $Fe + Fe_2O_3$
- mẫu thử tan là $FeO + Fe_2O_3$
$Fe + 2HCl \to FeCl_2 + H_2$
$FeO + 2HCl \to FeCl_2 + H_2O$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
Cho từ từ bột $Cu$ vào dung dịch sau phản ứng của các mẫu thử ở thí nghiệm trên :
- mẫu thử nào tan là $Fe + Fe_2O_3$
$2FeCl_3 + Cu \to 2FeCl_2 +CuCl_2$
- mẫu thử không tan là $Fe + FeO$


PTHH: C2H2 + 2Br2 -> C2H2Br4
Mol: 0,1 <--- 0,2
nCH4 = 3,36/22,4 = 0,15 (mol)
%VCH4 = 0,15/(0,1 + 0,15) = 60%
%VC2H2 = 100% - 60% = 40%

a) Gọi x, y lần lượt là số mol Al, Fe
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Fe + H2SO4 → FeSO4+ H2
\(\left\{{}\begin{matrix}27x+56y=5,54\\\dfrac{3}{2}x+y=\dfrac{3,584}{22,4}\end{matrix}\right.\)
=> x=0,06 , y =0,07
=> \(m_{Al}=1,62\left(g\right);m_{Fe}=3,92\left(g\right)\)
b) \(n_{H_2SO_4\left(pứ\right)}=n_{H_2}=0,16\left(mol\right)\)
=> \(m_{H_2SO_4\left(pứ\right)}=0,16.98=15,68\left(g\right)\)
c) \(m_{ddH_2SO_4}=\dfrac{15,68}{20\%}=78,4\left(g\right)\)
c) 2NaOH + H2SO4 → Na2SO4 + 2H2O
\(n_{H_2SO_4\left(dư\right)}=\dfrac{1}{2}n_{NaOH}=\dfrac{1}{2}.0,25.0,6=0,075\left(mol\right)\)
=> \(m_{H_2SO_4\left(bđ\right)}=15,68+0,075.98=23,03\left(g\right)\)









\(\left(1\right)Cu+2H_2SO_4\left(d\right)\rightarrow\left(t^o\right)CuSO_4+SO_2+2H_2O\\ \left(2\right)CuSO_4+Fe\rightarrow FeSO_4+Cu\\ \left(3\right)FeSO_4+Zn\rightarrow ZnSO_4+Fe\\ \left(4\right)2Fe+3Cl_2\rightarrow\left(t^o\right)2FeCl_3\)