
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: p+e+n=36
mà p+e=2n
=> 2n+n =36
⇒ 3n=36
=> n=12
=> p+e=24
=>p=12;e=12
=> Nguyên tử là Magie( kí hiệu :Mg)
Theo bài ra ta có
p+e+n=36
2p+n=36(Do p=e)(1)
Mặt khác
2p=2n
2p-2n=0(2)
Từ 1 và 2 ta có hệ pt sau
\(\left\{{}\begin{matrix}2p+n=36\\2p-2n=0\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=e=12\\n=12\end{matrix}\right.\)
Vậy Đây là nguyên tử Mg

nKMnO4 = 14,2/158 ≃ 0,0899 mol
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,0899 \(\dfrac{0,0899\times5}{2}\)
→ nCl2 = 0,22475 mol → VCl2 = 22,4.nCl2 = 5,0344 lít






Câu 16:
PTHH: \(Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{Cl_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\\n_{NaOH}=\dfrac{600\cdot20\%}{40}=3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) 2 chất p/ứ hết
Mặt khác: \(m_{Cl_2}=1,5\cdot71=106,5\left(g\right)\)
\(\Rightarrow m_{nướcjaven}=m_{Cl_2}+m_{ddNaOH}=706,5\left(g\right)\)

Nguyên tử nguyên tố X có số khối là 81. Trong nguyên tử, số hạt không mang điện chiếm 39,66% tổng số hạt. Xác định số lượng mỗi loại hạt và viết kí hiệu nguyên tử.
Nguyên tử nguyên tố X có số khối là 81
=>2p+n=81
Trong nguyên tử, số hạt không mang điện chiếm 39,66% tổng số hạt
=>39,66=100.n\81
=>n=32,4
sô lẻ vậy em kiểm tra lại đề bài
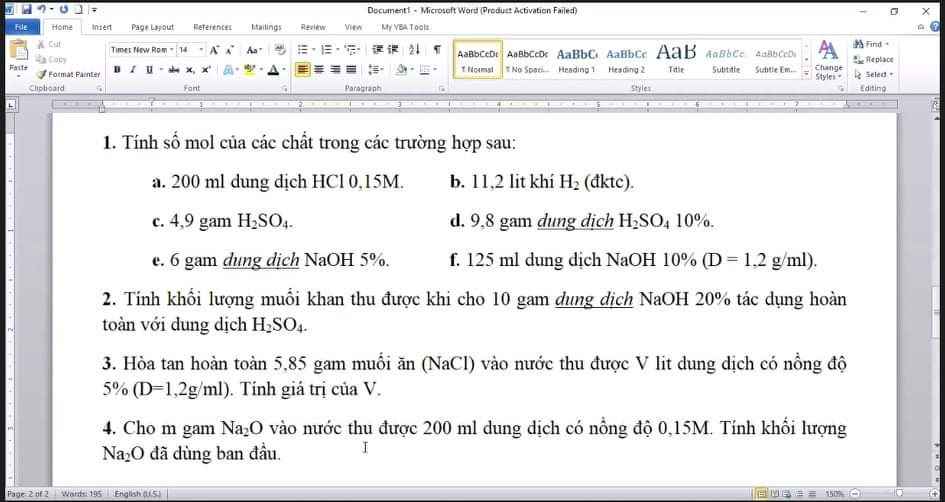








1.
a.\(n_{HCl}=0,2.0,15=0,03\left(mol\right)\)
b.\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
c.\(n_{H_2SO_4}=\dfrac{4,9}{98}=0,05\left(mol\right)\)
d.\(m_{H_2SO_4}=10\%.9,8=0,98\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{0,98}{98}=0,01\left(mol\right)\)
e.\(m_{NaOH}=6.5\%=0,3\left(g\right)\Rightarrow n_{NaOH}=\dfrac{0,3}{40}=0,0075\left(mol\right)\)
f.\(m_{ddNaOH}=125.1,2=150\left(g\right)\Rightarrow m_{NaOH}=150.20\%=30\left(g\right)\)
\(\Rightarrow n_{NaOH}=\dfrac{30}{40}=0,75\left(mol\right)\)
2.
\(m_{NaOH}=10.20\%=2\left(g\right)\Rightarrow n_{NaOH}=\dfrac{2}{40}=0,05\left(mol\right)\)
PTHH: 2NaOH + H2SO4 → Na2SO4 + H2O
Mol: 0,05 0,025
\(\Rightarrow m_{Na_2SO_4}=0,025.142=3,55\left(g\right)\)
3.
\(n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\)
PTHH: 2NaCl + 2H2O → 2NaOH + Cl2 + H2
Mol: 0,1 0,1
\(m_{NaOH}=0,1.40=4\left(g\right)\Rightarrow m_{ddNaOH}=\dfrac{4.100\%}{5\%}=80\left(g\right)\)
\(\Rightarrow V_{ddNaOH}=\dfrac{80}{1,2}=66,7\left(ml\right)\)