
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


C12:
\(nK=\dfrac{19,5}{39}=0,5\left(mol\right)\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
0,5 0,5 0,5 0,25 (mol)
mKOH = 0,5.56 = 28 (g)
m\(H_2=0,25.2=0,5\left(g\right)\)
mdd = mK + mddH2O - mH2
= 19,5 + 261 - 0,5 = 280 (g)
\(C\%_{dd}=\dfrac{28.100}{280}=10\%\)
=> Chọn D
II. Tự luận
C1 :
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
C2 :
\(N_2O_5+H_2O\rightarrow2HNO_3\)
=> Pứ hóa hợp
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
=> Pứ thế
C3:
Trích mẫu thử ở mỗi dung dịch , đánh số thứ tự , ta nhúng quỳ :
+ Quỳ chuyển đỏ : HCl
+ Quỳ chuyển xanh : NaOH
+ Quỳ không chuyển màu : NaCl
C4:
\(nCuO=\dfrac{2,4}{80}=0,03\left(mol\right)\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,03-->0,03--->0,03-->0,03
\(VH_2=0,03.22,4=0,672\left(l\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,02 0,03 (mol)
\(mAl=0,02.27=0,54\left(g\right)\)




Câu 5:
- Nước trong ấm đun bằng đất sẽ nhanh sôi hơn vì đất có nhiệt dung riêng nhỏ hơn nhôm (880 < 800) nên sẽ dễ dàng nóng lên và truyền nhiệt vào để đun sôi nước
Câu 6:
\(m_{H_2O}=1.1,5=1,5\left(kg\right)\\ m_{Al}=400g=0,4kg\\ \Delta t^o=100^oC-20^oC=80^oC\)
Nhiệt độ để đun sôi ấm nước là:
\(\)\(Q_{tổng}=Q_{Al}+Q_{H_2O}\\ =m_{Al}.c_{Al}.\Delta t^o+m_{H_2O}.c_{H_2O}.\Delta t^o\\ =0,4.880.80+1,5.4200.80\\ =532160\left(J\right)\)

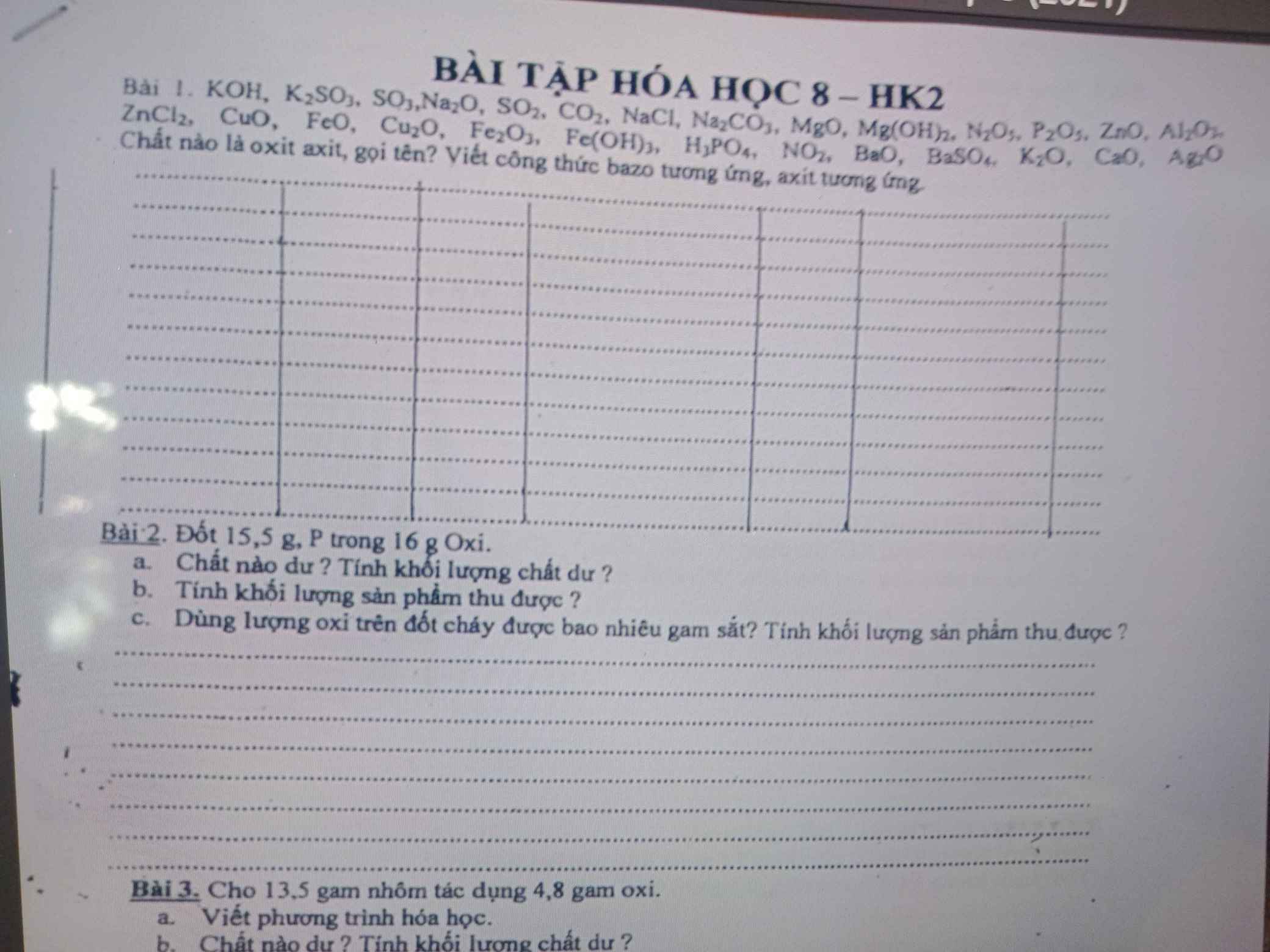
Bài 1: Oxit axit:
\(SO_3:\) Sulfur trioxide, axit tương ứng: \(H_2SO_4\)
\(SO_2\): Sulfur dioxide, axit tương ứng: \(H_2SO_3\)
\(CO_2:\) Carbon dioxide, axit tương ứng: \(H_2CO_3\)
\(N_2O_5:\) Dinitrogen pentoxide, axit tương ứng: \(HNO_3\)
\(P_2O_5:\) Phosphorus pentoxide, axit tương ứng: \(H_3PO_4\)
\(NO_2:\) Nitrogen dioxide, axit tương ứng: \(HNO_3\)
tất cả đều là oxit axit trừ:
\(NaCl;Na_2CO_3;MgO;Mg\left(OH\right)_2;Na_2O_3\\ ;ZnO;ZnCl_2;Fe\left(OH\right)_3;H_3PO_4;BaSO_4;Ag_2O;K_2SO_3\)
gọi tên của các oxit axit:
KOH:Kali hydroxide
SO3:Lưu huỳnh trioxide
Na2O: Natri oxide
mấy tên còn lại bn cứ theo cách gọi mà làm nhe , gọi tên nó theo 2345 j ấy rồi thêm oxide vô nha.

11. \(xFe_2O_3+\left(3x-2y\right)H_2\underrightarrow{t^o}2Fe_xO_y+\left(3x-2y\right)H_2O\)
14. \(Fe_2O_3+6HNO_3\rightarrow2Fe\left(NO_3\right)_3+3H_2O\)
17. \(2KMnO_4+8HCl\rightarrow2KCl+2MnCl_2+Cl_2+4H_2O\)
26. \(8Al+30HNO_3\rightarrow8Al\left(NO_3\right)_3+3NH_4NO_3+9H_2O\)

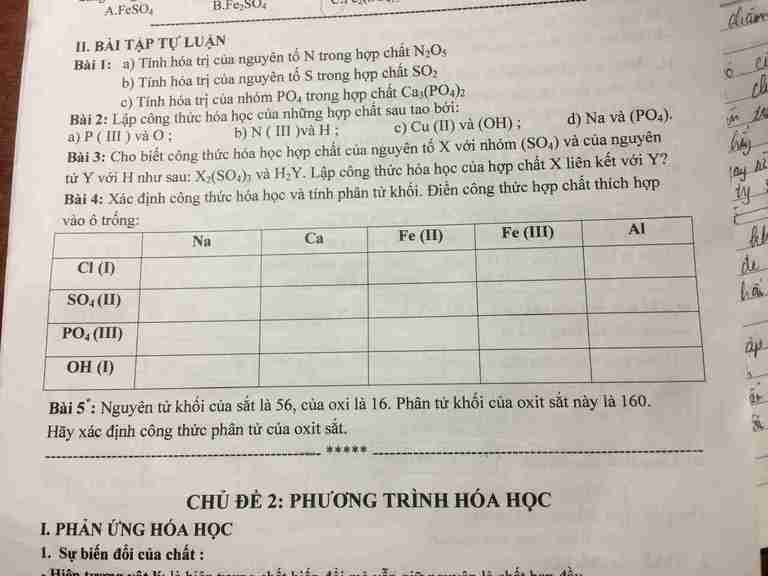
Bài 2: CTHH của câu d là Na3PO4
Bài 4:
| Na | Ca | Fe(II) | Fe(III) | Al | |
| Cl(I) | NaCl 58,5 | CaCl2 111 | FeCl2 127 | FeCl3 162,5 | AlCl3 133,5 |
| SO4 (II) | Na2SO4 142 | CaSO4 136 | FeSO4 152 | Fe2(SO4)3 400 | Al2(SO4)3 342 |
| PO4 (III) | Na3PO4 164 | Ca3(PO4)2 310 | Fe3(PO4)2 358 | FePO4 151 | AlPO4 122 |
| OH (I) | NaOH 40 | Ca(OH)2 74 | Fe(OH)2 90 | Fe(OH)3 107 | Al(OH)3 78 |







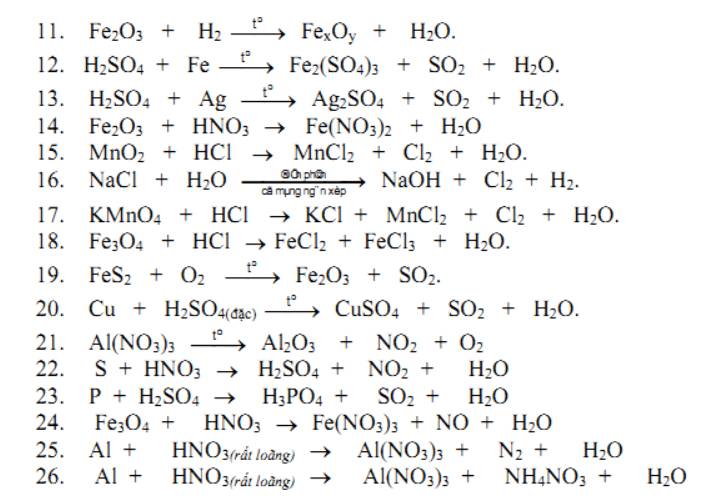

\(n_{HCl} = \dfrac{4,38}{36,5} = 0,12(mol)\)
Phương trình hóa học :
\(Fe_xO_y + 2yHCl \to xFeCl_{\dfrac{2y}{x}} + yH_2O\)
Theo PTHH :
\(n_{Fe_xO_y} = \dfrac{n_{HCl}}{2y} = \dfrac{0,06}{y}\ mol\\ \Rightarrow \dfrac{0,06}{y}.(56x + 16y) = 3,2\)
⇔ \(\dfrac{x}{y} = \dfrac{2}{3}\)
Vậy CTHH của oxit sắt : \(Fe_2O_3\)