
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Na2O: natri oxit - oxit bazơ
CO2: cacbon đioxit - oxit axit
Na2SO4: natri sunfat - muối trung hòa
HNO3: axit nitric - axit
Mg(OH)2: magie hiđroxit - bazơ
Ba(HCO3)2 : bari hiđrocacbonat - muối axit
Ca3(PO4)2: canxi photphat - muối trung hòa
H2SO3: axit sunfurơ - axit
P2O5: điphotpho pentaoxit - oxit axit
H3PO4: axit photphoric - axit
Fe(OH)3: sắt hiđroxit - bazơ
CuO: đồng (II) oxit - oxit bazơ
AgNO3: Bạc nitrat - muối trung hòa
K2CO3: kali cacbonat - muối trung hòa

\(n_{H_2}=0,3\left(mol\right);n_{O_2}=0,75\left(mol\right);n_{N_2}=0,8\left(mol\right);n_{CO_2}=0,15\left(mol\right)\)
a) \(\Sigma n=0,3+0,75+0,8+0,15=2\left(mol\right)\)
\(\%n_{H_2}=\dfrac{0,3}{2}.100=15\%\)
\(\%n_{O_2}=\dfrac{0,75}{2}.100=37,5\%\)
\(\%n_{N_2}=\dfrac{0,8}{2}.100=40\%\)
\(\%n_{CO_2}=\dfrac{0,15}{2}.100=7,5\%\)
b) \(\overline{M}_X=\dfrac{m_X}{n_X}=\dfrac{0,3.2+0,75.32+0,8.28+0,15.44}{2}=26,8\)(g/mol)
dX/SO2=\(\dfrac{26,8}{64}=0,41875\)
dX/H2S=\(\dfrac{26,8}{34}=0,788\)
dX/NO2=\(\dfrac{26,8}{46}=0,582\)
dX/NO=\(\dfrac{26,8}{30}=0,893\)

a) Canxi cacbonat \(\xrightarrow[]{t^o}\) Canxi oxit + Cacbon dioxit
b) \(m_{CaCO_3}=m_{CaO}+m_{CO_2}\)
c) áp dụng định luật bảo toàn khối lượng, ta có:
\(m_{CaCO_3}=m_{CaO}+m_{CO_2}\)
\(=56+44\)
\(=\) \(100\left(kg\right)\)
vậy khối lượng Canxi cacbonat cần dùng là \(100kg\)

a) kẽm + Oxi \(\xrightarrow[]{t^o}\) \(ZnO\)
b) \(m_{Zn}+m_{O_2}=m_{ZnO}\)
c) áp dụng định luật bảo toàn khối lượng, ta có:
\(m_{Zn}+m_{O_2}=m_{ZnO}\)
\(13+m_{O_2}=16,2\)
\(\Rightarrow m_{O_2}=16,2-13=3,2\left(g\right)\)
vậy khối lượng Oxi đã phản ứng là \(3,2g\)


CTTQ: Y2O
Ta có: 2MY + 16 = 2,9375 . 32
=> MY = 39
Y là Kali (K)
M hợp chất = 94

2Al+6HCl->2AlCl3+3H2
0,2----0,6-----0,2-----0,3
n Al=0,2 mol
n HCl =0,8 mol
=->Hcl dư
->m AlCl3=0,2.133,5=26,7g
->m HCl=0,2.36,5=7,3g
->VH2=0,3.22,4=6,72l
=>ntH2=0,3.6.1023=1,8.1023pt
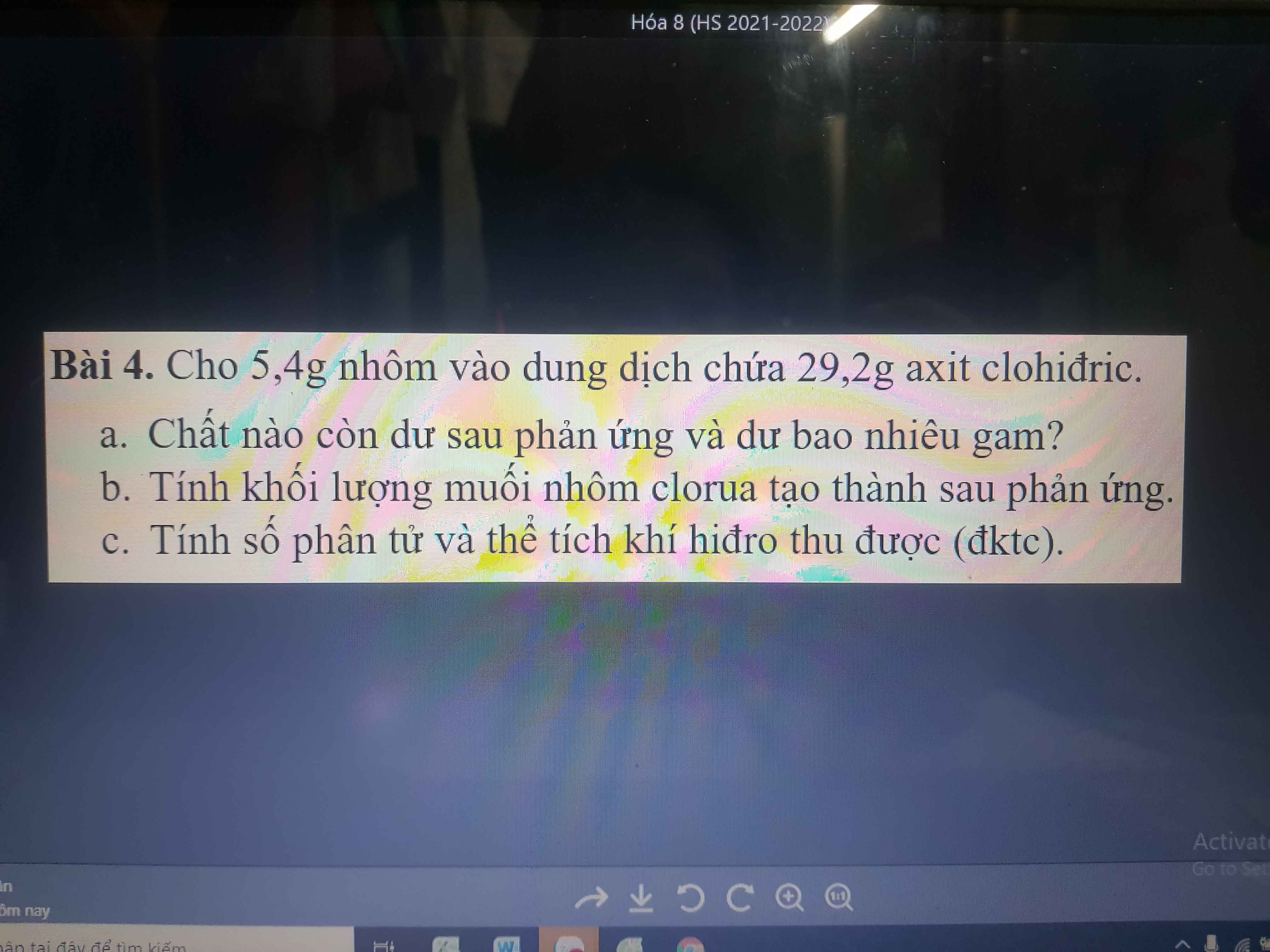
nAl = 5,4: 27 = 0,2 (mol)
nHCl = 29,2 : 36,5 = 0,8 (mol)
pthh: 2Al+ 6HCl ---> 2AlCl3 + 3H2
LTL :
0,2/2 < 0,8/6
=> HCl du
Al +








a) lưu huỳnh + Oxi \(\xrightarrow[]{t^o}\) lưu huỳnh dioxit
b) \(m_S+m_{O_2}=m_{SO_2}\)
c) áp dụng định luật bảo toàn khối lượng, ta có:
\(m_S+m_{O_2}=m_{SO_2}\)
\(3,2+m_{O_2}=6,4\)
\(\Rightarrow m_{O_2}=6,4-3,2=3,2\left(g\right)\)
vậy khối lượng Oxi đã phản ứng là \(3,2g\)