
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 8:
Đặt CTTQ oxit kim loại hóa trị III là A2O3 (A là kim loại)
nH2SO4=0,3(mol)
mNaOH=24%. 50= 12(g) => nNaOH=0,3(mol)
PTHH: 2 NaOH + H2SO4 -> Na2SO4 + 2 H2O
0,3________0,15(mol)
A2O3 +3 H2SO4 -> A2(SO4)3 +3 H2
0,05___0,15(mol)
=> M(A2O3)= 8/0,05=160(g/mol)
Mặt khác: M(A2O3)=2.M(A)+ 48(g/mol)
=>2.M(A)+48=160
<=>M(A)=56(g/mol)
-> Oxit cần tìm: Fe2O3
Bài 7:
mHCl= 547,5. 6%=32,85(g) => nHCl=0,9(mol)
Đặt: nZnO=a(mol); nFe2O3=b(mol) (a,b>0)
PTHH: ZnO +2 HCl -> ZnCl2+ H2O
a________2a_______a(mol)
Fe2O3 + 6 HCl -> 2 FeCl3 + 3 H2O
b_____6b____2b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}81a+160b=28,15\\2a+6b=0,9\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,15\\b=0,1\end{matrix}\right.\)
=> mFe2O3=0,1.160=16(g)
=>%mFe2O3=(16/28,15).100=56,838%
=>%mZnO= 43,162%

Tác dụng với \(H_2O:\)\(Na_2O,SO_3,P_2O_5,BaO,N_2O_5,SiO_2\)
Tác dụng với \(H_2SO_4:Na_2O,CuO,Al_2O_3,Fe_3O_4,BaO,MgO\)
Tác dụng với NaOH: \(SiO_2,P_2O_5,N_2O_5,SO_3\)


Câu 2 :
Trích một ít chất rắn làm mẫu thử :
Cho các chất rắn hòa tan vào nước :
+ Tan : CaO
+ Không tan : Al2O3 , Al
Pt : \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Cho dung dịch NaOH vào 2 mẫu thử không tan :
+ Tan và có khí thoát ra : Al
Pt : \(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
+ Tan : Al2O3
Pt : \(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
Chúc bạn học tốt

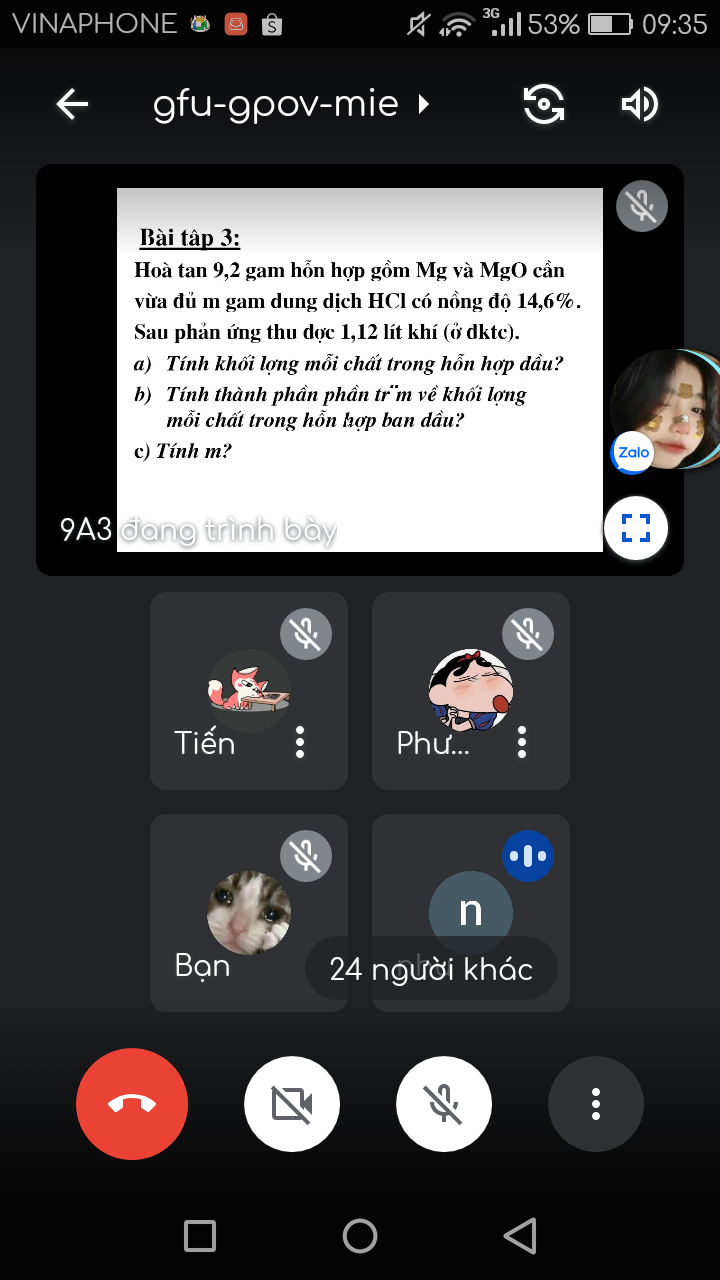
Ta có: \(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH:
Mg + 2HCl ---> MgCl2 + H2 (1)
MgO + 2HCl ---> MgCl2 + H2O (2)
a. Theo PT(1): \(n_{Mg}=n_{H_2}=0,05\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,05.24=1,2\left(g\right)\)
\(\Rightarrow m_{MgO}=9,2-1,2=8\left(g\right)\)
b. Từ câu a, suy ra:
\(\%_{m_{Mg}}=\dfrac{1,2}{9,2}.100\%=13,04\%\)
\(\%_{m_{MgO}}=100\%-13,04\%=86,96\%\)
c. Ta có: \(n_{MgO}=\dfrac{8}{40}=0,2\left(mol\right)\)
\(\Rightarrow n_{hh}=0,2+0,05=0,25\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_{hh}=2.0,25=0,5\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,5.36,5=18,25\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{18,25}{m_{dd_{HCl}}}.100\%=14,6\%\)
\(\Rightarrow m=m_{dd_{HCl}}=125\left(g\right)\)


Ta có: \(V_r=\dfrac{90.50}{100}=45\left(ml\right)\)
\(\Rightarrow70=\dfrac{45}{V_{hh\left(70^o\right)}}.100\Rightarrow V_{hh\left(70^o\right)}=64,3\left(ml\right)\)
Đáp án: C

a)
$2Ca + O_2 \xrightarrow{t^o} 2CaO$
$CaO + H_2O \to Ca(OH)_2$
$Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O$
$CaCO_3 + CO_2 + H_2O \to Ca(HCO_3)_2$
$Ca(HCO_3)_2 \xrightarrow{t^o} CaCO_3 + CO_2 + H_2O$
$Ca(HCO_3)_2 + 2HCl \to CaCl_2 + 2CO_2 + 2H_2O$
$CaCl_2 + Na_2CO_3 \to 2NaCl + CaCO_3$

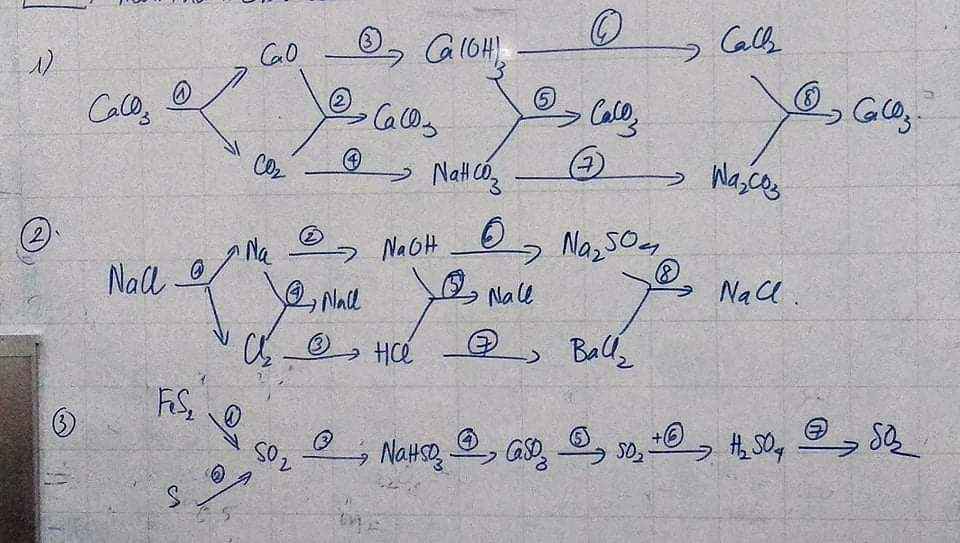
Chuỗi 3:
(1) \(4FeS_2+11O_2\xrightarrow[]{t^o}2Fe_2O_3+8SO_2\)
(2) \(S+O_2\xrightarrow[]{t^o}SO_2\)
(3) \(SO_2+NaOH\rightarrow NaHSO_3\)
(4) \(2NaHSO_3+Ca\left(OH\right)_2\rightarrow CaSO_3+Na_2SO_3+2H_2O\)
(5) \(CaSO_3+2HCl\rightarrow CaCl_2+H_2O+SO_2\uparrow\)
(6) \(SO_2+\dfrac{1}{2}O_2+H_2O\rightarrow H_2SO_4\)
(7) \(2H_2SO_{4\left(đ\right)}+S\xrightarrow[]{t^o}3SO_2+2H_2O\)
Chuỗi 2:
(1) \(NaCl\xrightarrow[nóng.chảy]{điện.phân}Na+\dfrac{1}{2}Cl_2\)
(2) \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
(3) \(Cl_2+H_2\xrightarrow[]{a/s}2HCl\)
(4) \(Na+\dfrac{1}{2}Cl_2\xrightarrow[]{t^o}NaCl\)
(5) \(NaOH+HCl\rightarrow NaCl+H_2O\)
(6) \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
(7) \(2HCl+BaO\rightarrow BaCl_2+H_2O\)
(8) \(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4\)


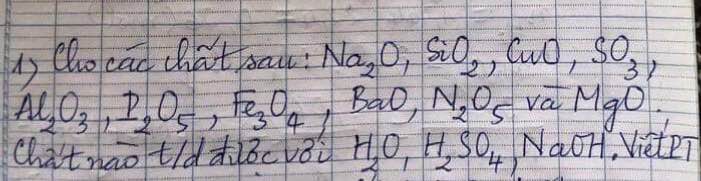
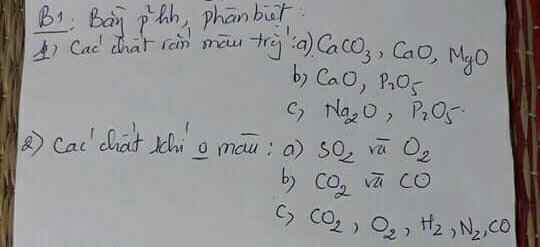



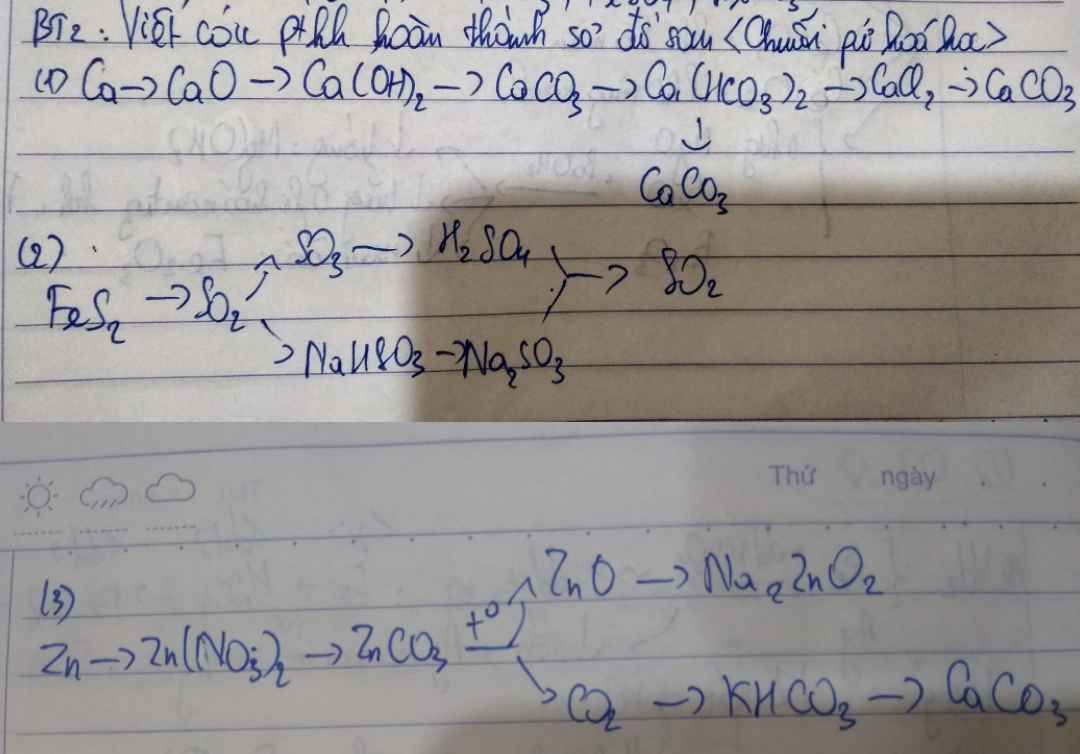
\(a,(1)Fe(NO_3)_3+3NaOH\to Fe(OH)_3\downarrow+3NaNO_3\\ (2)2Fe(OH)_3\xrightarrow{t^o}Fe_2O_3+3H_2O\\ (3)Fe_2O_3+3CO\xrightarrow{t^o}2Fe+3CO_2\\ (4)Fe+2HCl\to FeCl_2+H_2\\ b,(1)4Al+3O_2\xrightarrow{t^o}2Al_2O_3\\ (2)Al_2O_3+6HCl\to 2AlCl_3+3H_2O\\ (3)AlCl_3+3NaOH\to Al(OH)_3\downarrow+3NaCl\\ (4)2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ (5)2Al_2O_3\xrightarrow[cryolite]{đpnc}4Al+3O_2\\ (6)2Al+6HCl\to 2AlCl_3+3H_2\)