Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Do có khí CO2 sinh ra mà H+ hết nên Y chỉ có HCO3- và không có CO32-. (Do cho từ từ đến hết axit vào 2 muối cacbonat)
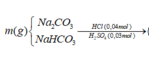
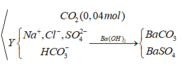
![]()
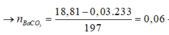
![]()
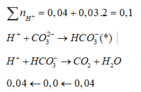
Mặt khác, n(H+) = 0,1 → n(H+) (*) = 0,06 → n(CO32-) = n(HCO3- (*)) = 0,06
→ n(Na2CO3) = 0,06 và n(NaHCO3) = 0,04 → m = 9,72


Phản ứng với Ba(OH)2 →kết tủa gồm: 0,3 mol BaCO3 và 0,1 mol BaSO4
→ m = 82,4g
V CO 2 = 2 , 24 lít
Đáp án C

+ Tính các giá trị đã biết:
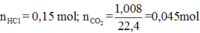
+ Với bài toán tổng hợp như này, thì ta phải viết các phương trình cụ thể cho dễ quan sát:
(1) H+ + CO3- ⟶ HCO3-
(2) H+ + HCO3- ⟶ CO2 +H2O.
Vì thu được khí CO2 nên có xảy ra phản ứng (2) ⇒ CO32- đã phản ứng hết với H+.
+ Từ
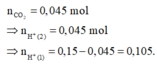
+ Vì khi thêm dung dịch Ba(OH)2 vào dung dịch Y thu được kết tủa nên trong Y phải có muối HCO3-
Như vậy suy ra ngay HCl đã phản ứng hết
Do đó từ (1) và (2) ta suy ra
![]()
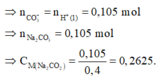
Loại ngay các đáp án A và B.
Việc cần thực hiện bây giờ là đi tính nồng độ của KHCO3 trong dung dịch X:
Vậy dung dịch Y chỉ chứa các ion K+, Na+, HCO3- và Cl-.
+ Khi thêm dịch Ba(OH)2 dư vào dung dịch Y thì:
![]()
Sau đó thì
![]()
+ Do đó 29,55 gam kết tủa là BaCO3:
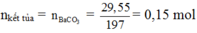
Ta sử dụng Bảo toàn nguyên tố C, toàn bộ C trong dung dịch Y chuyển hóa hết về trong kết tủa (vì thêm dung dịch Ba(OH)2 dư vào):
![]()
+ Lại áp dụng bảo toàn nguyên tốC ta được:
![]()
Hay ![]()
![]()
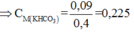
Đáp án D

200 ml dung dịch C chứa 0 , 2 mol CO 3 2 - 0 , 2 mol HCO 3 -
100 dung dịch D chứa 0 , 1 mol SO 4 2 - 0 , 3 mol H +
H+ + CO32- → HCO3-
0,2 ← 0,2 → 0,2
H+ + HCO3- → CO2 + H2O
0,1 → 0,1 → 0,1
⇒ V = 2,24 lít
Vậy dung dịch E còn (0,2 + 0,2 – 0,1) = 0,3 mol HCO3- và 0,1 mol SO42-
⇒ m = mBaCO3 + mBaSO4 = 0,3.197 + 0,1.233 = 82,4 ⇒ Chọn C.

Đáp án C
Dung dịch X chứa N 2 C O 3 Khi nhỏ từ từ dung dịch HCl vào X thì
![]()
![]()
Khi cho B a ( O H ) 2 dư vào dung dịch Y thì
n C O 2 = 0 , 05 m o l ; n B a C O 3 = 0 , 05 m o l
⇒ n N a 2 C O 3 = n C O 2 + n B a C O 3 = 0 , 1 m o l
Do đó M N a 2 C O 3 . x H 2 O = 186 ⇒ 106 + 18 x = 286
⇒ x = 10
⇒ V = 150 m l

Đáp án C
200ml dung dịch X chứa 0,15 mol Na2CO3 và 0,05 mol NaHCO3
Cho từ từ đến hết 200ml dung dịch H2SO4 vào 200 ml dung dịch X thấy thu được 0,15 mol CO2
Do vậy
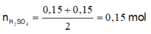
và còn dư 0,05 mol NaHCO3.
Cho Ba(OH)2 vào dung dịch Y thu được kết tủa gồm BaSO4 0,15 và BaCO3 0,05 mol.
→ m = 44,8

Đáp án B
Cho từ từ H + vào X thì phản ứng xảy ra theo thứ tự:
![]()
n C O 3 2 - = 0 , 1 m o l ; n H C O 3 - = 0 , 15 m o l ; n H + = 0 , 2 m o l
⇒ a = n C O 2 = n H + - n C O 3 2 - = 0 , 1 m o l

Đáp án B
► Cho "từ từ" H+ vào dung dịch hỗn hợp thì phản ứng xảy ra theo thứ tự:
H+ + CO32– → HCO3– || H+ + HCO3– → CO2 + H2O. Chú ý: bắt đầu có khí thoát ra.
||⇒ nH+ = nCO32– = 0,15 mol ⇒ x = 0,15 ÷ 0,1 = 1,5M. Bảo toàn nguyên tố Cacbon:
nNa2CO3 + nKHCO3 = n↓ ⇒ nKHCO3 = 0,1 mol ⇒ y = 0,1 ÷ 0,1 = 1M
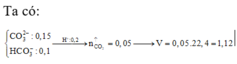
Ta có: X gồm \(\left\{{}\begin{matrix}HCO_3^-:0,1a\left(mol\right)\\CO_3^{2-}:0,1\left(mol\right)\end{matrix}\right.\) và Y gồm: \(\left\{{}\begin{matrix}H^+:0,2\left(mol\right)\\SO_4^{2-}:0,025\left(mol\right)\\Cl^-:0,15\left(mol\right)\end{matrix}\right.\)
- Nhỏ X vào Y:
\(HCO_3^-+H^+\rightarrow CO_2+H_2O\)
k.0,1a___k.0,1a___k.0,1a (mol)
\(CO_3^{2-}+2H^+\rightarrow CO_2+H_2O\)
k.0,1____2.k.0,1____k.0,1 (mol)
nH+ = k.0,1a + 2k.0,1 = 0,2
nCO2 = k.0,1a + k.0,1 = 0,12
\(\Rightarrow\dfrac{k.0,1a+2k.0,1}{k.0,1a+0,1k}=\dfrac{0,2}{0,12}\)
⇒ a = 0,5 (M)
- Nhỏ Y và X:
\(CO_3^{2-}+H^+\rightarrow HCO_3^-\)
0,1______0,1______0,1 (mol)
\(HCO_3^-+H^+\rightarrow CO_2+H_2O\)
__0,15___0,1_____0,1 (mol)
→ Z gồm: SO42-: 0,025 (mol) và HCO3-: 0,05 (mol)
- Cho Ba(OH)2 dư vào:
\(Ba^{2+}+SO_4^{2-}\rightarrow BaSO_4\)
_______0,025______0,025 (mol)
\(OH^-+HCO_3^-\rightarrow CO_3^{2-}+H_2O\)
_________0,05_____0,05 (mol)
\(Ba^{2+}+CO_3^{2-}\rightarrow BaCO_3\)
________0,05_______0,05 (mol)
⇒ m↓ = mBaSO4 + mBaCO3 = 15,675 (g) = m