Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có mC = 0,75m (gam) > 0,7m (gam)
\(\Rightarrow\) trong C có Fe dư
\(\Rightarrow\) HNO3 hết, trong B chỉ chứa muối Fe(NO3)2
PT:
Fe + 4HNO3 \(\rightarrow\)Fe(NO3)3 + NO + 2H2O
Fe + 6HNO3 \(\rightarrow\) Fe(NO3)3 + 3NO2 + 3H2O
Fe + 2Fe(NO3)3 \(\rightarrow\) 3Fe(NO3)2
Ta có : \(n_{hh}=\frac{2,87.1,2}{0,082.\left(273+27\right)}=0,14mol\)
\(\Rightarrow\) số mol HNO3 tạo muối = 0,44 – 0,14 = 0,3 (mol)
\(\Rightarrow\) \(n_{Fe\left(NO_3\right)_2}=0,15mol\)
\(\Rightarrow\) Khối lượng muối trong B = 0,15.180 = 27 (gam)
\(\Rightarrow\) nFe (pu) = 0,15 (mol) => mFe(pu) = 0,15.56 = 8,4 (gam)
\(m=\frac{8,4.100}{25}=33,6\left(g\right)\)

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

tính m, hay m1. mà tớ k thấy có m đâu hết cả?
m là khối lượng hỗn hợp hả bạn?
bạn yêu à...chúng ta sẽ giải hệ pt.
viết pt.. 2FeO + 10H2SO4 → Fe2(SO4)3+ 4H20+ SO2
x( mol)=>2x 1/2 x
2 Fe3O4+ 10H2SO4→3Fe2(SO4)3+10H2O+SO2
y(mol)=> 5y 1/2 y
từ đó => hệ{x+y=(224:1000/22.4)/0.5= 0.02
{2x+5y=0,07
=> x=y=0,01......
bạn tự tính tiếp đi nhá
kq: m=3,04 và m1=8( bảo toàn nguyên tố, rồi bảo toàn khối lượng) là ok.....![]()
e xin các anh các chị e đăng bài lên để hỏi chứ k phải để nói chuyện nếu ai muốn nói chuyện thì vao mà kp face vs e

Số mol các chất là:
![]()
![]()
Lượng Fe phản ứng tối đa => Thu được khí H2 và dung dịch sau phản ứng chỉ có ![]()
![]()
![]()
![]()
![]()
![]()
Các quá trình tham gia của H+:
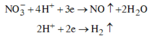
![]()
![]()
![]()
![]()
Đáp án D

Bạn chú ý, gửi từng câu hỏi một, không nên gửi nhiều câu hỏi một lúc
Câu 1.
Bài này có thể gọi M là kim loại chung của 3 kim loại trên:
M + HNO3 ---> M(NO3)n + NO + N2O + H2O (chú ý với bài tính toán kiểu này ko cần cân bằng pt).
Ta có số mol HNO3 = 1,5.0,95 = 1,425 mol.
Ta có khối lượng của hh khí (NO và N2O) = 16,4.2.số mol = 16,4.2.0,25 = 8,2 gam.
Áp dụng ĐLBTKL ta có: 29 + 63.1,425 = m + 8,2 + 18.0,7125 (chú ý số mol H2O luôn bằng 1/2 số mol HNO3).
Tính ra m = 97,75 g

đề là 0,05 h2..mới đúng ..có h2..thì tìm đk o-..rồi bảo toàn e là ra

Đáp án B