Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Đặt \(\hept{\begin{cases}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{cases}}\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\) (1)
\(Al+6HNO_3-->Al\left(NO_3\right)_3+3NO_2+3H_2O\) (2)
\(Cu+4HNO_3-->Cu\left(NO_3\right)_2+2NO_2+2H_2O\) (3)
Theo pthh (1) : \(n_{Al}=\frac{2}{3}n_{H_2}=0,2\left(mol\right)\) => \(x=0,2\left(mol\right)\)
Theo ptr (2); (3) : \(n_{NO_2}=3n_{Al}+2n_{Cu}\)
=> \(0,8=0,2\cdot3+2\cdot n_{Cu}\)
=> \(n_{Cu}=0,1\left(mol\right)\)
=> \(a=0,2\cdot27+0,1\cdot64=11,8\left(g\right)\)
b) PTHH : \(NH_3+HNO_3-->NH_4NO_3\) (4)
\(3NH_3+3H_2O+Al\left(NO_3\right)_3-->Al\left(OH\right)_3\downarrow+3NH_4NO_3\) (5)
\(2NH_3+2H_2O+Cu\left(NO_3\right)_2-->Cu\left(OH\right)_2\downarrow+2NH_4NO_3\) (6)
BT Al : \(n_{Al\left(OH\right)_3}=n_{Al}=0,2\left(mol\right)\)
BT Cu : \(n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
=> \(m\downarrow=m_{Al\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=25,4\left(g\right)\)
c) Gọi tên KL là X .
PTHH : \(2Al\left(NO_3\right)_3-t^o->Al_2O_3+6NO_2+\frac{3}{2}O_2\) (7)
\(Cu\left(NO_3\right)_2-t^o->CuO+2NO_2+\frac{1}{2}O_2\) (8)
\(4NO_2+O_2+2H_2O-->4HNO_3\) (9)
\(3X+4nHNO_3-->3X\left(NO_3\right)_n+nNO+2nH_2O\) (10)
viết ptr rồi, nhưng mik có thắc mắc là cho khí B hấp thụ vô nước => tính đc số mol của hno3, rồi áp vô X là ra, nhưng đề lại cho số mol NO =((( hoặc có thể dùng số mol NO để tính nhưng như thế có hơi thừa ko ? tính ra theo 2 cách thì cx ra 2 kq khác nhau ? ai githich giùm mik, hay mik tính sai hoặc phân tích đề sai nhỉ ?? :D

Em viết sơ đồ thôi ạ
3C2H4 +2 KMnO4 +4H2O =>3C2H4(OH)2 +2MnO2 +2KOH
a mol =>a mol
3CH2=CHOCH3 +2KMnO4 +4 H2O=>3CH2(OH)CH(OH)-O-CH3
a mol =>a mol
+2MnO2 +2KOH
CH3CHO + KMnO4 =>CH3COOK
a mol =>a mol
mcác chất hữu cơ=62a+92a+98a=12,6=>a=0,05 mol
Ta có C2H4 CH3CHO CH2=CH-O-CH3 mỗi chất 0,05 mol mà mỗi chất đều phản ứng với H2 tỉ lệ mol1:1 nên nH2=0,05.3=0,15 mol=>VH2=0,15.22,4=3,36 lit chọnA

Đáp án B
![]()
Vì sau phản ứng còn dư kim loại nên trong dung dịch B tồn tại Fe(NO3)2. Các phản láng xảy ra:
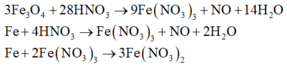
Như vậy trong toàn bộ các quá trình, số oxi hóa của sắt trong Fe và Fe3O4 đều về số oxi hóa +2.

Theo định luật bảo toàn mol electron, ta có:
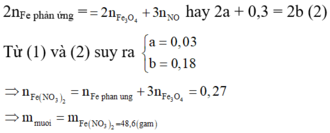

Đáp án A
n C O 2 = 0 , 1 m o l ; n K 2 C O 3 = 0 , 02 m o l
Cho toàn bộ Y tác dụng với BaCl2 dư thu được 0,06 mol kết tủa BaCO3.
Do vậy trong Y chứa 0,06 mol K2CO3.
Bảo toàn C nên Y còn chứa 0,06 mol KHCO3.
Bảo toàn nguyên tố K:
n K O H = 0,06.2 + 0,06 - 0,02.2 = 0,14 => x = 1,4


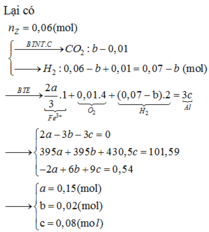
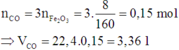
\(C_2H_5Br+KOH\underrightarrow{^{t^0,C_2H_5OH}}KBr+C_2H_4+H_2O\)
\(0.1....................................................0.1\)
\(V_{C_2H_4}=0.1\cdot22.4=2.24\left(l\right)\)
học giỏi phết