
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

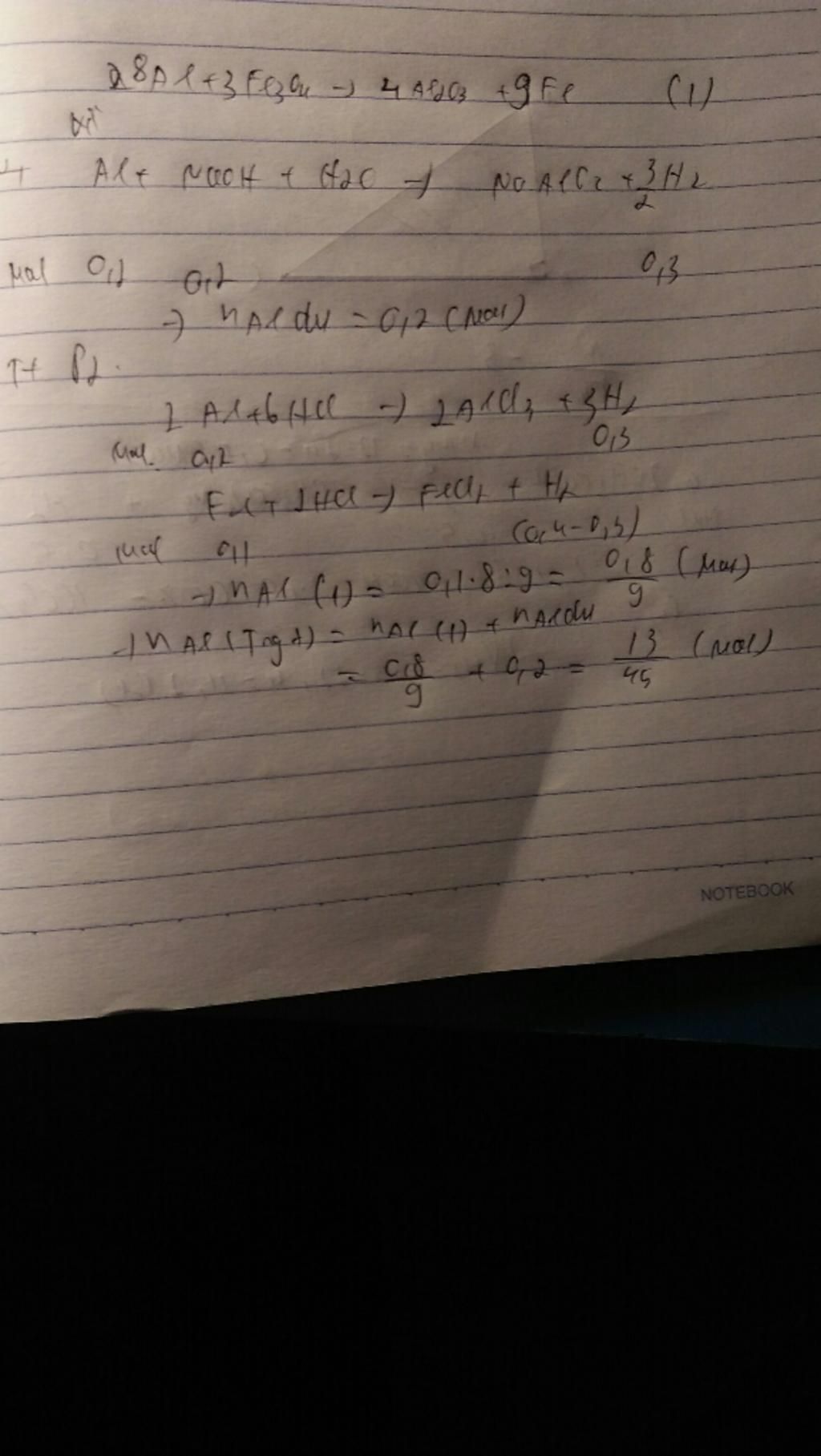

Vì Y tác dụng với NaOH sinh ra khí H 2 nên có Al còn dư → Fe2O3 phản ứng hết.
Vậy Y gồm có Al dư, Al2O3 và Fe.
- Y tác dụng với NaOH sinh khí H 2 .
2Al + 2NaOH + 2H2O
→ 2NaAlO2 + 3 H 2 (1)
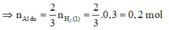
- Y tác dụng với HCl sinh khí H 2 .
2Al + 6HCl → 2 A l C l 3 +3 H 2 (2)
Fe + 2HCl → F e C l 2 + H 2 (3)
⇒ n H 2 (2) = 3/2 n A l d u = 3/2 . 0,2 = 0,3 mol
⇒ n H 2 (3) = n F e = n H 2 - n H 2 (2)
= 0,4-0,3= 0,1 mol
- Phản ứng nhiệt nhôm:
2Al + F e 2 O 3 → A l 2 O 3 + 2Fe (4)
Theo phản ứng (4) ta có:
⇒ n A l b đ = n A l d u + n A l p ư
= 0,2+0,1 = 0,3 mol⇒ Chọn A.

5/
-P/ư nhiệt Al
Fe2O3+ 2Al -----> 2Fe+ Al2O3 (1)
-Vì có khí H2 thoát ra chứng tỏ Al dư
Al+ NaOH+ H2O ------> NaAlO2+ 3/2H2 (2)
0.2......................................................0.3
2Al+ 6HCl --------> 2AlCl3+ 3H2 (3)
4/15....0.8..................4/15.......0.4
Do đó tổng mol Al trong X
ΣnAl=0.2+4/15 = 7/15 mol

các bạn trả lời nhanh dùm mình đi! mình đang cần gấp lắm! làm ơn!

$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}.0,15 = 0,1(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} + n_{Mg} = 0,35(mol)$
$\Rightarrow n_{Mg} = 0,35 - 0,15 = 0,2(mol)$
Vậy số mol Mg và Al là 0,2 và 0,1

Do Cu ko phản ứng với HCl ở điều kiện thường
=> 6,72 lít khí là sản phẩm của Al tác dụng với HCl
Ta có: nH2 = 6,72 / 22,4 = 0,3 mol
PTHH: 2Al + 6HCl ===> 2AlCl3 + 3H2
0,2 <== 0,3
=> mAl = 0,2 x 27 = 5,4 gam
Và 3,2 gam chất rắn ko tan chính là Cu
Khi cho hỗn hợp trên tác dụng với H2SO4 đặc nóng
PTHH 3Al + 6H2SO4(đ, nóng) ===> Al2(SO4)3 + 3SO2 + 6H2O
0,2 0,2
Cu + 2H2SO4 ===> CuSO4 + SO2 + 2H2O
0,05 0,05
nCu = 3,2 / 64 = 0,05 mol
=> VSO2 (đktc)= (0,05 + 0,2) x 22,4 = 5,6 lít