Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

4FeS2 + 11O2 => 2 Fe2O3 + 8SO2
SO2 +Ba(OH)2=> BaSO3 + H2O
0,15 mol<=0,15 mol
2SO2 +Ba(OH)2 => Ba(HSO3)2
x mol=>0,5x mol=>0,5x mol
mBa(OH)2=85,5 gam=>nBa(OH)2=0,5 mol
nBaSO3=0,15 mol
=>x=0,7 mol
tổng nSO2=0,7+0,15=0,85 mol =>nFeS2=0,425 mol=>m=0,425.120=51 gam
mdd X=0,7.64+200-32,55=212,25 gam
mBa(HSO3)2=0,5.0,7.299=104,65 gam
C% dd X=104,65/212,25.100%=49,31%
cho mình hỏi tại sao khi tính khối lượng dung dịch X không trừ khối lượng của nước

Tính được nBa(OH)2= nKOH= 0,2 mol; nBaSO3= 0,15 mol
Dung dịch Y + NaOH → Kết tủa →chứng tỏ Y có Ba(HSO3)2
Vậy sau phản ứng có các muối BaSO3, Ba(HSO3)2, KHSO3
(Không thể có K2SO3 hoặc kiềm dư vì chúng đối kháng với Ba(HSO3)2)
Các phương trình hóa học:
2FeS2 + 11/2 O2 → Fe2O3+ 4SO2 (1)
SO2+ Ba(OH)2 → BaSO3 + H2O (2)
0,15 0,15 0,15 mol
2SO2 + Ba(OH)2 →Ba(HSO3)2 (3)
0,1 ← (0,2-0,15) mol
SO2+ KOH → KHSO3 (4)
0,2 0,2 mol
Tổng số mol SO2 là 0,15 + 0,1+ 0,2= 0,45mol
Theo PT (1): nFeS2= 0,5. nSO2=0,225 mol → mFeS2= 0,225. 120 = 27 gam
*Tk
Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa
=>Dung dịch Y hình thành đồng thời SO32- và HSO3-
Ta có : nBaSO3 = 0,1 mol < nBa(OH)2 =0,15 mol
=>Kết tủa tính theo SO32- :0,1 mol
SO2 + 2OH- → SO32- + H2O
0,1......0,2......0,1
SO2 + OH- → HSO3-
0,2........(0,4-0,2)
=> nSO2 = 0,3 mol
Bảo toàn nguyên tố S: \(n_{SO_2}=n_{FeS_2}.2\)
=> nFeS2 = 0,15 mol
=> m = 18 gam.

\(n_{NaOH}=2.0,03=0,06\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=2.0,02=0,04\left(mol\right)\)
\(n_{CaCO3}=\dfrac{3}{100}=0,03\left(mol\right)\)
Thứ tự các pthh :
\(C+O_2-t^o->CO_2\) (1)
\(CO_2+Ca\left(OH\right)_2-->CaCO_3+H_2O\) (2)
\(CO_2+2NaOH-->Na_2CO_3+H_2O\) (3)
\(CO_2+Na_2CO_3-->2NaHCO_3\) (4)
\(CO_2+CaCO_3-->Ca\left(HCO_3\right)_2\) (5)
Vì \(n_{CaCO3}< n_{Ca\left(OH\right)2}\left(0,03< 0,04\right)\) => Có 2 giá trị của CO2 thỏa mãn
TH1: CO2 thiếu ở pứ 2 => Chỉ xảy ra pứ (1) và (2) => Không có pứ hòa tan kết tủa
Theo pthh (2) : \(n_{CO_2}=n_{CaCO3}=0,03\left(mol\right)\)
Bảo toản C : \(n_C=n_{CO2}=0,03\left(mol\right)\)
=> m = 0,03.12 = 0,36 (g)
TH2 : CO2 dư ở pứ (2) ; (3); (4), đến pứ (5) thì thiếu => Có pứ hòa tan kết tủa
Xét pứ (2); (3); (4) ; (5) :
\(\Sigma n_{CO2}=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+n_{Na2CO3}+n_{CaCO3\left(tan\right)}\)
\(=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+\dfrac{1}{2}n_{NaOH}+\left(n_{CaCO3\left(sinh.ra\right)}-n_{CaCO3thu.duoc}\right)\)
\(=n_{Ca\left(OH\right)2}+n_{NaOH}+\left(n_{Ca\left(OH\right)2}-0,03\right)\)
\(=2n_{Ca\left(OH\right)2}+n_{NaOH}-0,03\)
\(=2.0,04+0,06-0,03\)
\(=0,09\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,09\left(mol\right)\)
\(\Rightarrow m=0,09.12=1,08\left(g\right)\)
Em làm đúng rồi đấy nhưng TH 2 bước cuối chắc tính nhầm kìa nCO2 = 0,11 mol , e sửa lại nhé.

\(4FeS_2+11O_2\rightarrow\left(t^o\right)2Fe_2O_3+8SO_2\) (1)
\(n_{Ba\left(OH\right)_2}=0,2.1=0,2\left(mol\right)\)
\(n_{BaSO_3}=\dfrac{32,55}{217}=0,15\left(mol\right)\)
`@`TH1: Chỉ tạo ra kết tủa
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3\downarrow+H_2O\)
0,15 0,15 ( mol )
Theo ptr (1): \(n_{FeS_2}=\dfrac{n_{SO_2}}{2}=\dfrac{0,15}{2}=0,075\left(mol\right)\)
\(m_{FeS_2}=0,075.120=9\left(g\right)\)
`@` TH2: Ba(OH)2 hết
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3\downarrow+H_2O\)
0,2 ( mol )
0,15 0,15 0,15 ( mol )
\(Ba\left(OH\right)_2+2SO_2\rightarrow Ba\left(HSO_3\right)_2\)
0,05 0,1 ( mol )
Theo ptr (1): \(n_{FeS_2}=\dfrac{n_{SO_2}}{2}=\dfrac{0,15+0,1}{2}=0,125\left(mol\right)\)
\(n_{FeS_2}=0,125.120=15\left(g\right)\)

MX = 48 → nX = 0,96/48 = 0,02
Ta có:
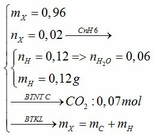
CO2 + Ba(OH)2 → BaCO3 + H2O
0,05 ←0,05 → 0,05
CO2 + BaCO3 + H2O → Ba(HCO3)2
0,02→ 0,02
Dư: 0,03
→ nBaCO3 dư = 0,03 → x = 5,91 (g) và mdd giảm = mBaCO3 – mCO2 + mH2O= 1,75 (g)





2FeS2 + \(\frac{11}{2}O_2\rightarrow Fe_2O_3+4SO_2\) (1)
Ba(OH)2 + SO2 \(\rightarrow\)BaSO3 + H2O (2)
nBaSO3=\(\frac{32,55}{217}=0,15mol\)
Ta có:
nBa(OH)2=\(\frac{200.42,75\%}{171}=0,5mol\)
=>nBa(OH)2 dư=0,5-0,15=0,35 mol
=> Nồng độ phần trăn dd X(Ba(OH)2 dư) là C%=\(\frac{0,35.171}{200}100\%=29,93\%\)
Ta có:
nSO2(2)=nSO2(1)=nBaSO3=0,15 mol
nFeS2=\(\frac{1}{2}\)nSO2(1)=0,075 mol
=> m=0,075.120= 9 (g)