Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nCaCO3 = 30/100 = 0.3 mol
Ca(OH)2 + CO2 --> CaCO3 + H2O
__________0.3_______0.3
m dung dịch giảm = mCaCO3 - (mCO2 + mH2O ) = 6
<=> 30 - (mH2O + 0.3*44) = 6
<=> mH2O = 10.8 g
<=> nH2O = 0.6 mol
2CxHy + (4x + y)O2 -to-> 2xCO2 + yH2O
________________________2x______y
________________________0.3______0.6
<=> 0.6*2x = 0.3y
<=> x/y = 1/4
CTHH : CH4

Đun nóng dd xuất hiện kết tủa chứng tỏ có Ca(HCO3)2
n Ba(OH)2 = 0,2(mol) ; n BaCO3 = 19,7/197 = 0,1(mol)
Ba(OH)2 + CO2 → BaCO3 + H2O
0,1...............0,1........0,1......................(mol)
Ba(OH)2 + 2CO2 → Ba(HCO3)2
0,1................0,2..................................(mol)
Suy ra: n CO2 = 0,1 + 0,2 = 0,3(mol)
Ta có:
m tăng = m CO2 + m H2O - m BaCO3
=> m H2O = 0,7 + 19,7 - 0,3.44 =7,2(gam)
=> n H2O = 7,2/18 = 0,4(mol)
Ta có :
n A = n H2O - n CO2 = 0,4 - 0,3 = 0,1(mol)
Số nguyên tử C trong A = n < n CO2 / n A = 0,3/0,1 = 3
Vậy n = 1 hoặc n = 2
Với n = 1 thì A là CH3OH không thể tách nước tạo anken => Loại
Với n = 2 thì A là C2H5OH => B là C2H4
$C_2H_4OH \xrightarrow{t^o,xt} C_2H_4 + H_2O$

\(n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\)
Đặt CTHH của X là \(C_xH_y\)
\(C_xH_y+\left(x+\dfrac{y}{4}\right)O_2\underrightarrow{t^o}xCO_2+\dfrac{y}{2}H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
\(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\)
\(m_{dd.giảm}=m_{kt}-\left(m_{CO_2}+m_{H_2O}\right)\\ \Leftrightarrow0,5=20-\left(m_{CO_2}+m_{H_2O}\right)\\ \Rightarrow m_{CO_2}+m_{H_2O}=20-0,5=19,5\left(g\right)\left(I\right)\)
Mặt khác:
\(m_{O_2}=m_{CO_2}+m_{H_2O}-m_X=19,5-4,3=15,2\left(g\right)\\ \Rightarrow n_{CO_2}+0,5n_{H_2O}=\dfrac{15,2}{32}=0,475\left(mol\right)\left(II\right)\)
Từ (I), (II) suy ra: \(\left\{{}\begin{matrix}n_{CO_2}=0,3\\n_{H_2O}=0,35\end{matrix}\right.\)
Vì \(n_{H_2O}>n_{CO_2}\Rightarrow X:ankan\) \(\left(C_nH_{2n+2}\right)\)
\(n=\dfrac{n_{CO_2}}{n_{H_2O}-n_{CO_2}}=\dfrac{0,3}{0,35-0,3}=6\)
a
CTPT của X: \(C_6H_{14}\)
b
\(V_{O_2}=0,475.22,4=10,64\left(l\right)\)
c
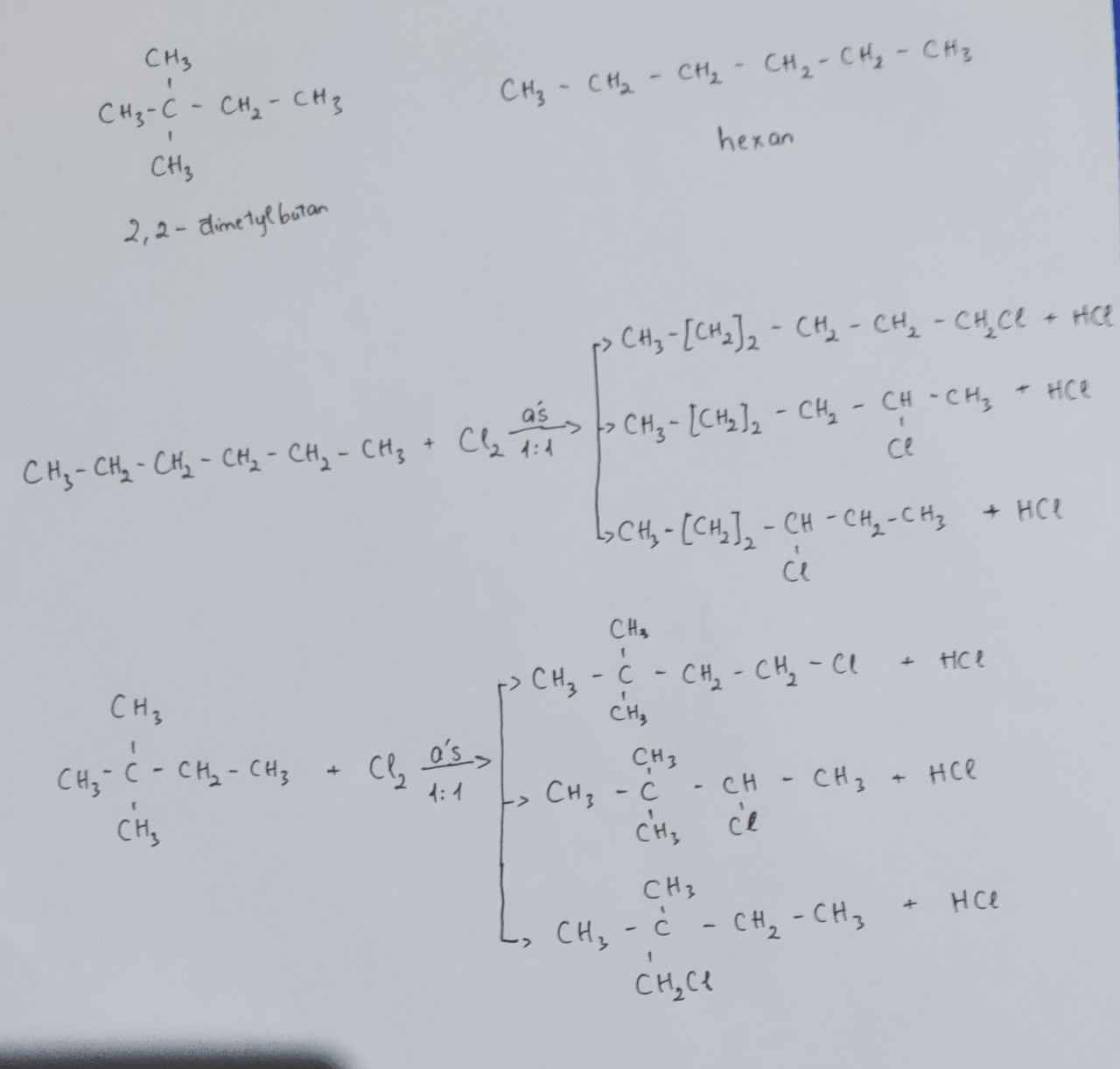
2,2-dimethylbutane thiếu 1 đồng phân monochloride ở C1 kìa bạn.

Ta có: m dd tăng = mCO2+H2O - mCaCO3 => mCO2+H2O = 25,4 + 10 = 35,4 gam
TH1: Ca(OH)2 dư, CaCO3 chưa bị hòa tan
CO2 + Ca(OH)2 → CaCO3, Ca(OH)2 dư, H2O
=> nCO2 = nCaCO3 = 0,1 mol => mH2O = 35,4 - 0,1.44 = 31 gam
=> nH2O = 1,722 mol > nCO2 (loại)
TH2: CaCO3 bị hòa tan một phần
CO2 + Ca(OH)2 → CaCO3, Ca(HCO3)2, H2O
BTNT "Ca": nCa(HCO3)2 = nCa(OH)2 - nCaCO3 = 0,35 - 0,1 = 0,25 mol
BTNT "C": nCO2 = nCaCO3 + 2nCa(HCO3)2 = 0,1 + 2.0,25 = 0,6 mol
=> mH2O = 35,4 - 0,6.44 = 9 gam => nH2O = 0,5 mol
=> n axit = nCO2 - nH2O = 0,6 - 0,5 = 0,1 mol
=> nO(axit) = 2naxit = 0,2 mol
=> m = m axit = mC + mH + mO = 0,6.12 + 0,5.2 + 0,2.16 = 11,4 gam

m H2O = m bình 1 tăng = 21,6(gam)
=> n H2O = 21,6/18 = 1,2(mol)
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
n CO2 = n CaCO3 = 100/100 = 1(mol)
Bảo toàn nguyên tố C,H :
n C = n CO2 = 1(mol)
n H = 2n H2O = 1,2.2 = 2,4(mol)
n C : n H = 1 : 2,4 = 5 : 12
Suy ra :CTP là (C5H12)n
Ta có :
M X = (12.5 + 12)n = 32.2,25
=> n = 1
Vậy CTPT là C5H12

Nhận thấy các chất trong hỗn hợp đều có dạng Cm(H2O)n nên có thể quy về C và H2O.
Đốt cháy hỗn hợp thu được sản phẩm dẫn vào Ba(OH)2 dư thu được kết tủa là BaCO3 0,47 mol nên C 0,47 mol.
Khối lượng dung dịch giảm 65,07 gam.
\(\rightarrow mH_2O=92,59-65,07-0,47.44=6,84\left(g\right)\)
\(\rightarrow m=6,84+0,47.12=12,48\left(g\right)\)
=> chọn D
nCO2 = nBaCO3 = 0,47 mol => nC = 0,47 mol
m dung dịch giảm = mBaCO3 – mCO2 – mH2O
=> 65,07 = 92,59 – 0,47.44 – mH2O
=> mH2O = 6,84 gam => nH2O = 0,38 mol => nH = 0,76 mol
CTPT các chất lần lượt là: C3H4O2, C2H4O2, C6H10O5
=> nO = n\(\dfrac{H}{2}\) = 0,38 mol
->m = mC + mH + mO = 0,47.12 + 0,76 + 0,38.16 = 12,48 gam

Câu 1.1 : Muối gồm NaHCO3(y mol) ; n Na2CO3(x mol)
Ta có :
106x + 84y = 42,2
2x + y = 0,65.2
=> x = 0,2 ; y = 0,25
=> n CO2 = x + y = 0,45(mol)
m H2O = 29,7 - 0,45.44 = 9,9(gam)
n H2O = 9,9/18 = 0,55(mol)
Gọi n CH4 = a(mol) ; n C2H4 = b(mol) ; n C2H2 = c(mol)
Ta có:
a + b + c = 0,3
a + 2b + 2c = 0,45
2a + 2b + c = 0,55
=> a = 0,15 ; b = 0,1 ; c = 0,05
%V CH4 = 0,15/0,3 .100% = 50%

Thuần đốt cháy :
⇒ nhìn hỗn hợp hiđrocacbon gồm a mol C + b mol H2.
Đốt cháy 1,84 gam hỗn hợp + O2 a mol CO2 + b mol H2O.
Ta có :
Ca(OH)2 dùng dư :
Δmdung dịch giảm = mCaCO3↓ – ∑(mCO2 + mH2O)
→Ta có: 100a – (44a + 18b) = 4,76
=>56a – 18b = 4,76. (1)
Lại có :
12a + 2b = mhỗn hợp = 1,84 (2)
Từ 1, 2=> a = 0,13; b = 0,14.
→ m gam kết tủa là 0,13 mol CaCO3 → m = 13,0 gam.
Ta có: \(n_{Ba\left(OH\right)_2}=0,4.1=0,4\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
TH1: Ba(OH)2 dư.
BTNT C, có: nCO2 = nBaCO3 = 0,15 (mol) = nC
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = 5,8 (g)
\(\Rightarrow n_{H_2O}=\dfrac{5,8}{18}=\dfrac{29}{90}\left(mol\right)\Rightarrow n_H=\dfrac{29}{45}\left(mol\right)\)
\(\Rightarrow x:y=0,15:\dfrac{29}{45}\approx23:100\) → vô lý
TH2: Ba(OH)2 hết.
BTNT Ba, có: nBa(HCO3)2 = 0,4 - 0,15 = 0,25 (mol)
BTNT C, có: nCO2 = 0,25.2 + 0,15 = 0,65 (mol)
Có: m dd giảm = mBaCO3 - mCO2 - mH2O ⇒ mH2O = -16,2 → vô lý
Bạn xem lại đề nhé.
Biết M CxHy =(28 g/mol) :)