Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Gọi công thức chung là CnH2n (n không nhỏ hơn 2)
\(n_{kt}=0,55mol=n_{CO_2}=n_{H_2O}\)
\(n_{anken\left(olefin\right)}=n_{Br_2}=0,25mol\)
=> n = 0,55 : 0,25 = 2,2
=> 2 olefin đó là C2H4 và C3H6.
a = 0,25(12.2,2 + 2.2,2) = 7,7 g
b. Gọi số mol C2H4, C3H6 trong hh lần lượt là u, v mol
n(hỗn hợp) = u + v = 0,25
m(hỗn hợp) = 28u + 42v = 7,7
=> u = 0,2; v = 0,05
=> %mC2H4 = 72,73%
=> %mC3H6 = 27,27%
anken nCo2 = nH20
- Ca(oh)2 dư => 55g kết tủa = CaCO3 => nCO2 = nH20 = 0.55 mol
=>> a = 0.55*(12+2) = ?
mol hỗn hợp = 0.25 mol => khối lượng trung bình = a / 0.25
=>> hỗn hợp

Benzen không cộng hợp với brom trong nước brom.
Xiclohexen có phản ứng:
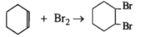
Số mol xiclohexen = số mol B r 2
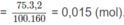
Đặt số mol benzen trong hỗn hợp M là x.
2 C 6 H 6 + 15 O 2 → 12 C O 2 + 6 H 2 O
x mol 6x mol
2 C 6 H 10 + 17 O 2 → 12 C O 2 + 10 H 2 O
015 mol 0,09 mol
C O 2 + C a ( O H ) 2 → C a C O 3 ↓ + H 2 O
6x + 0,09 = 0,210 ⇒ x = 0,02
Khối lượng hỗn hợp M là : 0,02.78 + 0,015.82 = 2,79 (g).
% về khối lượng của C 6 H 6 là:

⇒ C 6 H 10 chiếm 44,1% khối lượng hỗn hợp M.

Chất khí bay ra chính là metan ⇒ nCH4 = nCO2 = 5,544 : 44 = 0,126 mol
VCH4 = 0,126.22,4 = 2,8224 lít
⇒ %VCH4 = (2,8224 : 10,8 ).100% = 26,13%
⇒ %Volefin = 73,87%
Đáp án A

Đáp án B
Hướng dẫn
Phương trình phản ứng:
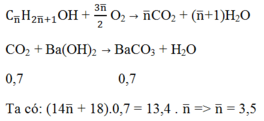
Vậy có 2 ancol no là C3H7OH và C4H9OH
Khi tách nước C3H7OH cho 1 sản phẩm duy nhất là CH2 = CH – CH3 . Như vậy 3 sản phẩm còn lại phải có 1 cặp là đồng phân hình học cis-trans và 1 sản phẩm phụ
=> C4H9OH phải là butan-2-ol.

a) \(n_{O_2}=\dfrac{21,056}{22,4}=0,94\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{52}{100}=0,52\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=n_{CaCO_3}=0,52\left(mol\right)\)
BTNT O: \(n_{H_2O}=2n_{O_2}-2n_{CO_2}=0,84\left(mol\right)\)
\(\Rightarrow n_{ankan}=n_{H_2O}-n_{CO_2}=0,32\left(mol\right)\)
\(\Rightarrow\text{Số }\overline{C}_{\text{trung bình}}=\dfrac{n_C}{n_{ankan}}=\dfrac{0,52}{0,32}=1,625\)
Vì 2 ankan liên tiếp nhau trong dãy đồng đẳng nên 2 ankan là CH4 (metan) và C2H6 (etan)
b) BTNT H: \(n_H=2n_{H_2O}=1,68\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_6}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_C=n_{CH_4}+2n_{C_2H_6}=a+2b=0,52\\n_H=4n_{CH_4}+6n_{C_2H_6}=4a+6b=1,68\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,12\\b=0,2\end{matrix}\right.\left(TM\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,12.16}{0,12.16+0,2.30}.100\%=24,24\%\\\%m_{C_2H_6}=100\%-24,24\%=75,76\%\end{matrix}\right.\)
c)
\(CH_4+Cl_2\xrightarrow[]{askt}CH_3Cl\left(\text{metyl clorua}\right)+HCl\\ C_2H_6+Cl_2\xrightarrow[]{askt}C_2H_5Cl\left(\text{etyl clorua}\right)+HCl\)

Đáp án A
hhX gồm CH4 và CnH2n
10,8 lít hhX + Br2 thấy có CH4 bay ra.
CH4 + O2 → 0,126 mol CO2
→ nCH4 = 0,126 x 22,4 = 2,8224 lít →
%
V
C
H
4
=
2
,
8224
10
,
8
≈
26
,
13
%
; %VCnH2n ≈ 73,87%

Đáp án C
nX =0,4 mol
Khối lượng bình 1 đựng P2O5 tăng là số lượng của H2O.
Khối lượng bình đựng KOH rắn tăng chính là khối lượng của CO2
Khi đốt cháy 1 anken ta luôn có: ![]()
![]()
![]()
![]() anken là C3H6 và C4H8
anken là C3H6 và C4H8
Gọi phần trăm thể tích về thể tích của C3H6 là x% thì phần trăm thể tích về thể tích của C4H8 là
(100 -x) %
Ta có:
![]()
![]()

a, Ta có: \(n_{CO_2}=n_{CaCO_3}=\dfrac{55}{100}=0,55\left(mol\right)\)
\(n_{hh}=n_{Br_2}=0,25.1=0,25\left(mol\right)\)
Gọi CTPT chung của 2 olefin là \(C_{\overline{n}}H_{2\overline{n}}\)
\(\Rightarrow\overline{n}=\dfrac{n_{CO_2}}{n_{hh}}=2,2\)
Mà: 2 olefin đồng đẳng kế tiếp.
→ C2H4 và C3H6.
\(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}+n_{C_3H_6}=0,25\\2n_{C_2H_4}+3n_{C_3H_6}=0,55\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{C_2H_4}=0,2\left(mol\right)\\n_{C_3H_6}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow a=m_{C_2H_4}+m_{C_3H_6}=0,2.28+0,05.42=7,7\left(g\right)\)
b, mC2H4 = 0,2.28 = 5,6 (g)
mC3H6 = 0,05.42 = 2,1 (g)
Có: nH2O = nCO2 = 0,55 (mol)
BTNT O, có: \(2n_{O_2}=2n_{CO_2}+n_{H_2O}\Rightarrow n_{O_2}=0,825\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,825.22,4=18,48\left(l\right)\)