Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi oxit kim loại phải tìm là MO và nCuO = a và nMO =2a
nHNO3 = 0.15 mol
Vì hiđro chỉ khử được những oxit kim loại đứng sau nhôm trong dãy điện hóa nên có 2 trường hợp xảy ra.
∙ Trường hợp 1: M đứng sau nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
MO + H2 → M + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3M + 8HNO3 → 3M(NO3)2 + 2NO + 4H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 16a/3 = 0.15 }
a = 0,01875 và M = 40 → M là Ca.
Trường hợp này loại vì CaO không bị khử bởi khí H2.
∙ Trường hợp 2: M đứng trước nhôm trong dãy điện hóa
CuO + H2 → Cu + H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
MO + 2HNO3 → M(NO3)2 + 2H2O
Ta có hệ pt:
{ 80a + (M +16).2a = 3.6
8a/3 + 4a = 0.15 }
a = 0,0225 và M = 24 → M là Mg → Đáp án C

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
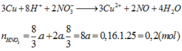
=>a=0,025=>80a+(M+16).2a=4,8
=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
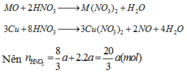
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24

Chọn đáp án C
Sơ đồ quá trình phản ứng:
C + H2O → hh X = {H2; CO; CO2} || X + a mol Fe3O4; b mol CuO → 25,92 gam hh Y.
(2a + 0,5b) mol H2 + hh Y → {Fe; Cu} + H2O.
Gọi số mol {CO; H2} trong X là z mol → cần đúng z mol O trong oxit đề → {CO2; H2O}.
→ 160a + 80b = 25,92 + 16z (1). Lại có để chuyển hết (3a + b) mol O trong oxit → {CO2; H2O}
thì cần vừa đủ z + 2a + 0,5b mol hh {CO; H2} → 3a + b = z + 2a + 0,5b ↔ a + 0,5b = z (2).
Từ (1) và (2) ta có z = 0,18 mol. Đến đây có 2 hướng xử lí:
ᴥ cách 1: thường các bạn sẽ tìm mối ràng buộc nữa thì C + H2O → CO + H2 || C + 2H2O → CO2 + 2H2.
Bằng cách gọi số mol C ở các pt lần lượt là x, y mol → 2x + 3y = 0,2 mol
và 2x + 2y = nhh CO + H2 0,18 mol. Giải tìm ra đáp án C. ♣.
Theo hướng này có thể nhanh hơn như sau: nCO2 = 0,2 - z = 0,02 mol.
Thay vào 2 phương trình trên cũng ra kết quả tương tự.
ᴥ cách 2: có thể đi theo hướng sau: hiểu rõ vấn đề + rút gọn suy nghĩ, cần hình dung:
C + H2O →....→.... cuối cùng sẽ thu được CO2 + H2O.
như vậy 0,18 mol O là ở trong CO2 luôn → có 0,09 mol C.
→ trong Y có 0,09 mol CO và CO2 (bảo toàn C) → có 0,11 mol H2O
→ mY = 0,09 × 44 + 0,11 × 18 - 0,18 × 16 = 3,06 gam. → dY/H2 = 3,06 ÷ 0,2 ÷ 2 = 7,65.
Chọn đáp án C. ♣
p/s: bài toán này khai thác điểm đặc biệt Fe2O3 và CuO có M = 160 và 80 + bản chất CO và H2 cùng nhận 1 O.

Chọn đáp án C
Đặt nCl2 = x; nO2 = y ⇒ nkhí = x + y = 0,25 mol. Bảo toàn khối lượng:
7,2 + 71x + 32y = 23 ||⇒ giải hệ có: x = 0,2 mol; y = 0,05 mol.
Gọi n là hóa trị của M. Bảo toàn electron: n × nM = 2nCl2 + 4nO2.
⇒ nM = 0,6 ÷ n ⇒ MM = 7,2 ÷ (0,6 ÷ n) = 12n.
⇒ n = 2 và MM = 24 ⇒ M là Magie (Mg) ⇒ chọn C.

Chọn đáp án A
Trong Y sẽ chứa các chất là: MgO; Cu; Al2O3 và Fe. Khí CO không khử được oxit của kim loại mạnh hơn Al, nên khí CO chỉ khử được CuO, FeO.
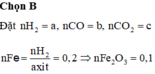
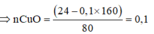

ta có Ax + 2By = 23.8 (1) ( dữ kiện : khối lượng hỗn hợp kim loại ) 3y = 0.6
3y = 0.6  x = 0.2
x = 0.2  A là Zn
A là Zn  x =0.6 y = 0.2/3
x =0.6 y = 0.2/3
x+ 3y = 0.8 ( dữ kiện : cần 8.96 lít O2 )
và có dữ kiện cuối cùng là hỗn hợp chất rắn sau khi bị khử bởi H2 còn lại 33.4 gam
thì ta tính đọc số mol Oxi còn trong hỗn hợp là 0.6
TH1 chỉ có A bị khử thì số mol oxi trong hỗn hợp trên là của B
mà B hóa trị 3 và không bị khủ thì chỉ có thể là Al
TH2 chỉ có B bị khử ta tính được số mol trong hỗn hợp trên là của A
ta tính : ráp số vào phương trình (1) ta được 0.6A +0.4/3B =23.8
từ đó ta có 23.8 / 0.6 < A,B< 23.8*3/0.4
lúc này ta lục bảng tuần hoàn và thế vô đều không thỏa mãn nên th2 loại
vậy kim loại cần tìm là Zn và Al