Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức phân tử của A, B là C x H y O
Phương trình hoá học:
C x H y O + (x +y/4 -1/2) O 2 → x CO 2 + y/2 H 2 O
n CO 2 = 17,6/44 = 0,4 mol; n H 2 O = 9/18 = 0,5 mol (1)
m C = 0,4.12 = 4,8 gam; m H = 0,5.2 = 1g (2)
Từ (1), (2)
→ x : y : 1 = 4,8/12 : 1/1 : 1,6/16 = 0,4 : 1 : 0,1
Vậy m O = 7,4 - 4,8 - 1,0 = 1,6 (gam)
=> Công thức phân tử của A, B là C 4 H 10 O
Ta có M A , B = 74 (g/mol)
n A , B = 7,4/74 = 0,1 mol
Khi phản ứng với Na có khí bay ra → trong A, B có nhóm OH.
Phương trình hoá học :
C 4 H 9 OH + Na → C 4 H 9 ONa + 1/2 H 2
Vậy số mol có nhóm OH là 2 n H 2 = 2. 0,672/22,4 = 0,06 < n A , B
→ trong A, B có 1 chất không có nhóm OH → Cấu tạo tương ứng là
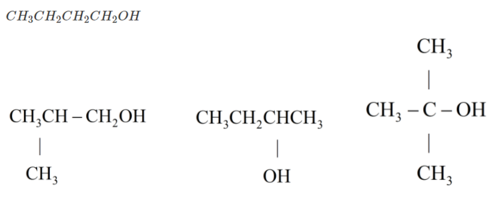
Chất không có nhóm OH :
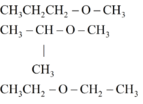

a.

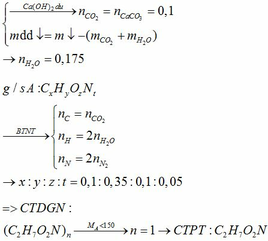
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)

Fe3O4+4CO=>3Fe+ 4CO2
CuO+CO=>Cu+CO2
Cr B gồm Fe Cu
HH khí D gồm CO dư và CO2
CO2 +Ca(OH)2=>CaCO3+H2O
p/100 mol<= p/100 mol
2CO2+Ca(OH)2 => Ca(HCO3)2
p/50 mol
Ca(HCO3)2+ 2NaOH=>CaCO3+ Na2CO3+2H2O
p/100 mol p/100 mol
Tổng nCO2=0,03p mol=nCO
=>BT klg
=>m+mCO=mCO2+mB=>mB=m+0,84p-1,32p=m-0,48p
c) hh B Fe+Cu
TH1: Fe hết Cu chưa pứ cr E gồm Ag Cu
dd Z gồm Fe(NO3)2
Fe+2Ag+ =>Fe2+ +2Ag
TH2:Cu pứ 1p cr E gồm Cu và Ag
Fe+2Ag+ => Fe2+ +2Ag
Cu+2Ag+ =>Cu2+ +2Ag
Dd Z gồm 2 muối của Fe2+ và Cu2+

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6

a) Mấu chốt ở chỗ chỉ số H bằng nhau
Đặt ankan M: CnH2n+2
→anken N: Cn+1H2n+2 (giải thích: anken có C = ½ H)
ankin P: Cn+2H2n+2 [giải thích: ankin có C = ½ (H + 2)]
·Xét TN đốt cháy hỗn hợp X:
nX = 0,4 mol; nCO2 = nCaCO3 = 0,7 mol
=> C trung bình =0,7: 0,4 = 1,75
=> Trong hỗn hợp có ít nhất một chất có số C < 1,75
=> n = 1
→M: CH4
N: C2H4 → CTCT: CH2=CH2
P: C3H4 → CTCT: CH≡C–CH3
b) Đặt CTTB: C1,75H4 (M=25)
=> số liên kết pi TB = 0,75
nX = 15 : 25 = 0,6mol
C1,75H4 + 0,75Br2 → C1,75H4Br1,5
0,6 → 0,45 (mol)
=> V = 450ml
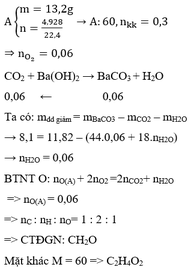
C chứa N2, O2
Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{O_2\left(dư\right)}=y\left(mol\right)\end{matrix}\right.\)
=> \(\overline{M}=\dfrac{28x+32y}{x+y}=15,2.2=30,4\left(g/mol\right)\)
=> 2,4x = 1,6y
=> 1,5x = y (1)
\(n_{H_2O}=\dfrac{9}{18}=0,5\left(mol\right)\)
Gọi số mol CO2 là z (mol)
=> \(x+y+z=\dfrac{14,56}{22,4}=0,65\left(mol\right)\) (2)
Bảo toàn C: nC(A) = z (mol)
Bảo toàn H: nH(A) = 1 (mol)
Bảo toàn N: nN(A) = 2x (mol)
\(n_{O_2\left(pư\right)}=\dfrac{13,44}{22,4}-y=0,6-y\left(mol\right)\)
Bảo toàn O: \(n_{O\left(A\right)}+2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
=> \(n_{O\left(A\right)}=2y+2z-0,7\left(mol\right)\)
Do mA = 15 (g)
=> 12z + 1 + 28x + 32y + 32z - 11,2 = 15
=> 28x + 32y + 44z = 25,2 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\\z=0,4\left(mol\right)\end{matrix}\right.\)
nC(A) = 0,4 (mol)
nH(A) = 1 (mol)
nO(A) = 0,4 (mol)
nN(A) = 0,2 (mol)
Xét nC(A) : nH(A) : nO(A) : nN(A) = 0,4 : 1 : 0,4 : 0,2 = 2 : 5 : 2 : 1
Mà A có 1 nguyên tử N
=> CTPT: C2H5O2N