
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

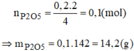

\(n_P=\dfrac{6.2}{31}=0.2\left(mol\right)\)
\(n_{O_2}=\dfrac{7.84}{22.4}=0.35\left(mol\right)\)
\(4P+5O_2\underrightarrow{^{^{t^0}}}2P_2O_5\)
\(4........5\)
\(0.2........0.35\)
\(LTL:\dfrac{0.2}{4}< \dfrac{0.35}{5}\Rightarrow O_2dư\)
\(m_{O_2\left(dư\right)}=\left(0.35-0.25\right)\cdot32=3.2\left(g\right)\)
\(m_{P_2O_5}=0.1\cdot142=14.2\left(g\right)\)
Tham khảo nha!!!
nP = 6,2/31 = 0,2 mol ; nO2 = 7,84/22,4 = 0,35 mol
a, PTHH : 4P + 5O2 (to) -> 2P2O5
0,2 0,35 mol
Ta thấy : 0,2/4 < 0,35/5 -> nO2 dư = 0,35 - 0,05*5 = 0,1 mol
-> mO2 dư = 0,1*32 = 3,2 gam
b, Theo pt : nP2O5 = 1/2*nP = 0,1 mol -> mP2O5 = 0,1*142 = 14,2 gam

a. \(n_{Mg}=\dfrac{m}{M}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: \(2Mg+O_2\rightarrow^{t^0}2MgO\)
-Theo PTHH: 2 1 2 (mol)
-Theo đề bài: 0,2 0,1 (mol)
-So sánh tỉ lệ số mol đề bài với số mol phương trình của Mg và O2 có:
\(\dfrac{0,2}{2}=\dfrac{0,1}{1}\)
\(\Rightarrow\) Mg và O2 phản ứng hết.
b. -Chất tạo thành: Magie oxit.
\(n_{MgO}=\dfrac{0,1.2}{1}=0,2\) (mol)
\(\Rightarrow m_{MgO}=n.M=0,2.40=8\left(g\right)\)

\(a) n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ \dfrac{n_P}{4} = 0,05 < \dfrac{n_{O_2}}{5}=0,06 \to O_2\ dư\\ n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)\\ m_{O_2\ dư} = (0,3 - 0,25).32 = 1,6(gam)\\ b) P_2O_5\ \text{được tạo thành}\\ n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)\\ m_{P_2O_5} = 0,1.142 = 14,2(gam)\)

ta có : nP=9,3:31=0,3 mol
nO=5,6:22,4=0,25 mol
PTHH: 5O2 + 2P\(\rightarrow\) 2P2O5
ban đầu: 0,25 0,3 (mol)
phản ứng: 0,25 \(\rightarrow\) 0,25 (mol)
sau phản ứng: 0 0,05 0,1 (mol)
vậy sau phản ứng O2 hết còn P dư
mP dư= 0,05.31=1,55 g
b) chất P2O5
mP2O5= 0,1.390=39 g

\(n_P=\dfrac{m_p}{M_P}=\dfrac{12,4}{31}=0,4mol\)
\(n_{O_2}=\dfrac{m_{O_2}}{M_{O_2}}=\dfrac{17}{32}=0,53125mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
4 5 2 ( mol )
0,4 0,53125 ( mol )
ta có: \(\dfrac{0,4}{4}< \dfrac{0,53125}{5}\)
=> Chất dư là \(O_2\)
\(n_{O_2\left(du\right)}=0,53125-0,5=0,03125mol\)
Chất được tạo thành là \(P_2O_5\)
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=\left(\dfrac{0,4.2}{4}\right).142=28,4g\)

nP = 7,44/31 = 0,24 (mol)
nO2 = 6,16/22,4 = 0,275 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5
LTL: 0,24/4 > 0,275/5 => P dư
nP2O5 = 0,275 : 5 . 2 = 0,11 (mol)
mP2O5 = 0,11 . 142 = 15,62 (g)
\(4P+5O_2->2P_2O_5\)
4 5 2
0,24 0,3 0,12 (mol)
\(n_P=\dfrac{m}{M}=\dfrac{7,44}{31}=0,24\left(mol\right)\)
\(m_{P_2O_5}=n\text{×}M=0,12\text{×}\left(31\text{×}2+16\text{×}5\right)=0,12\text{×}142=17,04\left(g\right)\)