Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải:
Số mol của P là:
nP = m/M = 0,2 (mol)
Số mol của O2 là:
nO2 = V/22,4 = 0,35 (mol)
PTHH: 4P + 5O2 -t0-> P2O52
ĐB: ----0,2---0,35--------------
PƯ: ----0,2------0,25-----0,05-
Spư:----0--------0,1-------0,05-
Theo phương trình ta thấy O2 còn dư, các chất còn lại tính theo P
Khối lượng sản phẩm thu được là:
mP2O5 = n.M = 0,05.142 = 7,1 (g)
Vậy ...
PTHH: 4P + 5O2 → 2P2O5
Theo bài ta có: nP(bđ) = mP / MP = 6,2 / 31 = 0,2 mol
nO2(bđ) = VO2 / 22,4 = 7,84 / 22,4 = 0,35 mol
Theo pthh ta có: nP(pt) = 4 mol ; nO2(pt) = 5 mol
Ta có tỉ lệ: \(\dfrac{nP_{bđ}}{nP_{pt}}\) = \(\dfrac{0,2}{4}\) = 0,05 mol < \(\dfrac{nO2_{bđ}}{nO2_{pt}}\) = \(\dfrac{0,35}{5}\) = 0,07 mol
Sau pư Photpho tgpư hết, Oxi còn dư
Theo pthh và bài ta có:
nO2(tgpư) = \(\dfrac{5}{4}\) . nP = \(\dfrac{5}{4}\) . 0,2 = 0,25 mol
=> nO2(dư) = nO2(bđ) - nO2(tgpư) = 0,35 - 0,25 =0,1 mol
⇒ mO2 = nO2 dư . MO2 = 0,1 . 32 = 3,2 g
nP2O5 = 1/2 . nP = 1/2 . 0,2 = 0,1 mol
⇒ mP2O5 = nP2O5 . MP2O5 = 0,1 . 142 = 14,2 g
Vậy.....

a+b, \(n_{Fe\left(đb\right)}=\frac{22,4}{56}=0,4\left(mol\right)\)
\(n_{O_{2\left(đb\right)}}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(3Fe+2O_2\rightarrow Fe_3O_4\)
Theo PTHH: 3mol 2mol
\(\frac{n_{Fe\left(đb\right)}}{n_{Fe\left(PTHH\right)}}\) \(\frac{n_{O_{2\left(đb\right)}}}{n_{O_{2\left(PTHH\right)}}}\)
\(\Rightarrow\frac{0,4}{3}>\frac{0,2}{2}\)
⇒ O2 hết; Fe dư
Theo PTHH: \(n_{Fe_3O_4}=\frac{1}{2}n_{O_2}=\frac{1}{2}.0,2=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4}=0,1.232=23,2\left(g\right)\)

a) PTHH: \(4P+5O_2 \underrightarrow{t^o} 2P_2O_5\)
b) Ta có: \(n_{P_2O_5}=\dfrac{28,4}{142}=0,2\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_P=0,4mol\\n_{O_2}=0,5mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_P=0,4\cdot31=12,4\left(g\right)\\V_{O_2}=0,5\cdot22,4=11,2\left(l\right)\end{matrix}\right.\)

a)
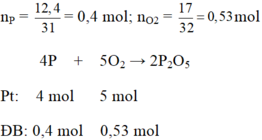
Xét tỉ lệ số mol đề bài với số mol phương trình của P và O2 ta có:

b) Chất tạo thành: đi photpho pentaoxit P2O5
Theo phương trình 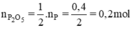
mP2O5 = n.M = 0,2.(31.2 + 16.5) = 28,4 (g)

\(n_P=\dfrac{m_P}{M_P}=\dfrac{12,4}{31}=0,4mol\)
\(n_{O_2}=\dfrac{m_{O_2}}{M_{O_2}}=\dfrac{17}{32}=0,53125mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
0,4 < 0,53125 ( mol )
0,4 0,5 0,2 ( mol )
\(n_{O_2\left(du\right)}=0,53125-0,5=0,03125mol\)
Chất được tạo thành là P2O5
\(m_{P_2O_5}=n_{P_2O_5}.M_{P_2O_5}=0,2.142=18,4g\)

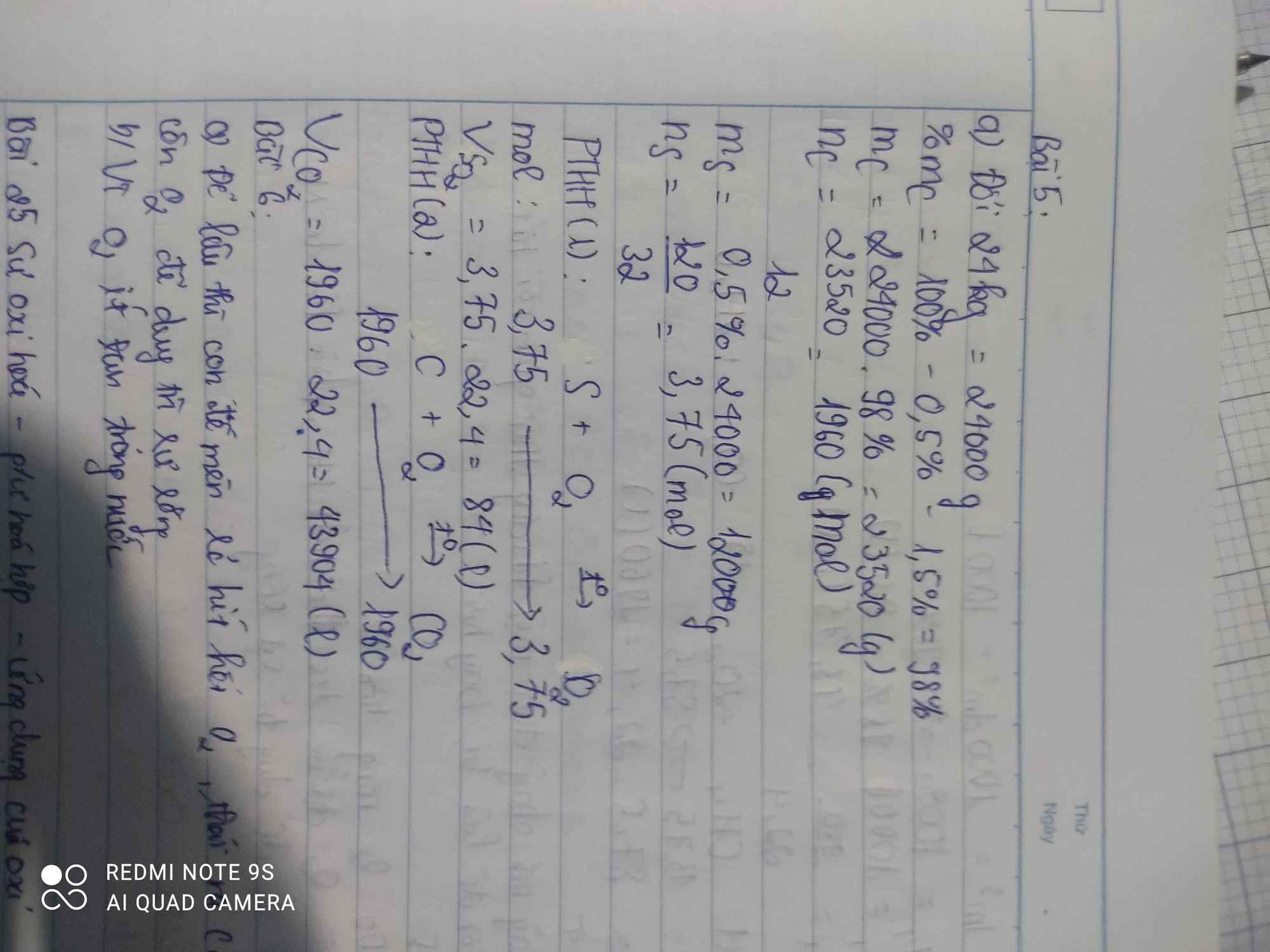
Bài 4:
a) \(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O_2}=\dfrac{17}{32}=0,53125\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
Xét tỉ lệ: \(\dfrac{0,4}{4}< \dfrac{0,53125}{5}\) => P hết, O2 dư
PTHH: 4P + 5O2 --to--> 2P2O5
0,4-->0,5--------->0,2
=> \(n_{O_2\left(dư\right)}=0,53125-0,5=0,03125\left(mol\right)\)
b) \(m_{P_2O_5}=0,2.142=28,4\left(g\right)\)

nP = 24.8 / 31 = 0.8 (mol)
nO2 = 34 / 32 = 1.0625 (mol)
4P + 5O2 -to-> 2P2O5
Bđ: 0.8.....1.0625
Pư: 0.8.........1...............0.4
KT : 0..........0.0625.........0.4
mO2 (dư) = 0.0625 * 32 = 2 (g)
mP2O5 = 0.4 * 142 = 56.8 (g)
PTHH: 4P + 5O2 -\(t^0\) --> 2P2O5
ta có n=m/M
=> nP =0,8 và nO2=2,125
theo pt có
nP/4=0,2 < nO2/5=0,425
=> Oxi dư
theo pt
\(\dfrac{nO2\left(pư\right)}{nP}=\dfrac{5}{4}\Rightarrow nO2\left(pư\right)=\dfrac{5}{4}\cdot0,8=1mol\)
nO2(dư)= 2,125-1=1,125mol
b, chất đc tạo thành là: đi photpho penta oxit
theo pt
\(\dfrac{nP2O5}{nP}=\dfrac{2}{4}\Rightarrow nP2O5=\dfrac{2}{4}\cdot0,8=0,4mol\)
ADCT: m=nM
=> mP2O5=0,4*142=56,8g

1)
nAl = 0,2 mol
nO2 = 0,1 mol
4Al (2/15) + 3O2 (0,1) ---to----> 2Al2O3 (1/15)
\(\dfrac{nAl}{4}=0,05>\dfrac{nO2}{3}=0,0333\)
=> Chọn nO2 để tính
- Các chất sau phản ứng gồm: \(\left\{{}\begin{matrix}Al_{dư}:0,2-\dfrac{2}{15}=\dfrac{1}{15}\left(mol\right)\\Al_2O_3:\dfrac{1}{15}\left(mol\right)\end{matrix}\right.\)
=> mAldư = 1/15 . 27 = 1,8 gam
=> mAl2O3 = 1/15 . 102 = 6,8 gam
(Câu 2;3;4 tương tự như vậy thôi )

\(n_{O_2}=\frac{0,1}{22,4}=\text{0,0045}\left(mol\right)\)
PTHH : \(4P+5O_2-^{t^o}\rightarrow2P_2O_5\)
Theo PT:4..........5........................
Theo ĐB:0,1....0,0045.....................
\(\Rightarrow\frac{0,1}{4}>\frac{0,0045}{5}\)
Vậy P dư, O2 phản ứng hết
Theo PT \(n_{P\left(p.ứ\right)}=\frac{0,0045.4}{5}=\text{0,0036}\left(mol\right)\)
\(\Rightarrow n_{P\left(dư\right)}=0,1-\text{0,0036}=\text{0,0964}\left(mol\right)\)
\(\Rightarrow m_{P\left(dư\right)}=\text{0,0964}.31=\text{2,9884}\left(g\right)\)