Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Ta có: \(n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)\(\Rightarrow n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow\%m_{CuO}=\dfrac{0,1\cdot80}{40}\cdot100\%=20\%\)
\(\Rightarrow\%m_{Fe_2O_3}=80\%\)

a, PTHH:
2Cu + O2 -> (t°) 2CuO (1)
CuO + H2 -> (t°) Cu + H2O (2)
2Na + 2H2O -> 2NaOH + H2 (3)
2H2 + O2 -> (t°) 2H2O (4)
b, A: CuO: đồng (II) oxit
B: Cu: đồng
C: H2O: nước
D: H2: hiđro
F: O2: oxi
c, nCu = 12,8/64 = 0,2 (mol)
Theo (1): nCuO = nCu = 0,2 (mol)
Theo (2): nH2O = nCuO = 0,2 (mol)
Theo (3): nH2 = nH2O/2 = 0,2/2 = 0,1 (mol)
Theo (4): nH2O = nH2 = 0,1 (mol)
mH2O = 0,1 . 18 = 1,8 (g)

\(a,n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2 (X là H2)
0,1-------------------------->0,1
b, \(n_{CuO}=\dfrac{9,6}{80}=0,12\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
LTL: 0,12 > 0,1 => CuO dư
hh chất sau pư: CuO, Cu
Theo pthh: nCuO (pư) = nCu = nH2 = 0,1 (mol)
=> \(\left\{{}\begin{matrix}m_{CuO\left(dư\right)}=\left(0,12-0,1\right).80=1,6\left(g\right)\\m_{Cu}=0,1.64=6,4\left(g\right)\end{matrix}\right.\)

Gọi $n_{Al}= a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 4,44(1)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
B gồm : $Al_2O_3, Fe$
$n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,5a(mol)$
Suy ra: $0,5a.102 + 56b = 5,4(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,06
$m_{Al} = 0,04.27 =1,08\ gam$
$m_{Fe} = 0,06.56 = 3,36\ gam$
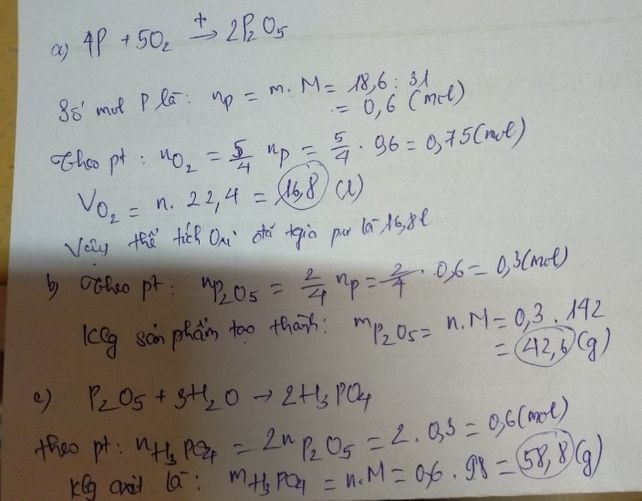
 Bạn tham khảo cách làm nhé! cho mik 1 like nha
Bạn tham khảo cách làm nhé! cho mik 1 like nha