Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giải thích: Đáp án A
ne = It/ F = 5. 96,5.60/96500 = 0,3 (mol)
Tại catot (-) Tại anot (+)
Cu2+ + 2e → Cu 2Cl- → Cl2 + 2e
0,5 a→ a → 0,5a 0,15 ← 0,3
2H2O + 2e → H2 + 2OH-
b → 0,5b

Nồng độ của CuSO4 = a = 0,2 M

Đáp án B
ne = It/F = 5.(96,5.60)/96500 = 0,3 mol
nCl- (0,5) > ne (0,3) => Cl- chưa bị điện phân ở anot.
Giả sử Cu2+ chưa bị điện phân hết => nCu = 0,3/2 = 0,15 mol
nCl2 = 0,3/2 = 0,15 mol
m dung dịch giảm = mCu+mCl2 = 0,15.64 + 0,15.71 = 20,15 gam => Loại
=> Cu2+ bị điện phân hết, H2O đã bị điện phân ở catot.
Catot:
Cu2+ + 2e → Cu
x → 2x →x
H2O + 1e → OH- + 0,5H2
0,3-2x → 0,15-x
Anot:
Cl- - 1e → 0,5Cl2
0,3→ 0,15
m dung dịch giảm = mCu + mH2 + mCl2 => 17,15 = 64x + 2(0,15-x) + 0,15.71 => x = 0,1mol
=> a = 0,1/0,5 = 0,2 mol/lít

Chọn A.
Ta có: ne = 0,4 mol. Tại thời điểm này tại catot có Cu (0,2 mol) và anot Cl2 (0,1a mol); O2 (b mol)
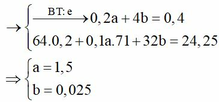

Giải thích: Đáp án D
Do dung dịch sau điện phân chứa 2 chất là: Na2SO4 và NaOH. Tỉ lệ mol CuSO4 và NaCl là 1:3 nên Cu2+ bị điện phân hết trước.
Al2O3+2OH- → 2AlO2-+H2O
=>nOH-=2nAl2O3=0,05 mol.
Quá trình điện phân:
Cu2+ + 2Cl- →Cu + Cl2
a 2a a a
2Cl- + 2H2O → Cl2 + H2 + 2OH-
a(=3a-2a) 0,5a 0,5a a=0,05
m giảm=64a+71a+71.0,5a+2.0,5a=8,575 gam<10,375
=> H2O bị điện phân: mH2O=10,375-8,575=1,8 gam
H2O→H2+0,5O2
0,1 0,1 0,05 mol
Tại anot: 0,075 mol Cl2, 0,05 mol O2
=> ne=0,075.2+0,05.4=0,35 mol=>t=ne.96500/I=0,35.96500/2,68=12602,6 giây=3,5 giờ.

Vì 2nCuSO4 < nNaCl ⇒ Al2O3 bị hòa tan bởi OH–.
Ta có nAl2O3 = 0,025 mol ⇒ nOH– cần dùng = 0,05 mol.
⇒ nNaOH = 0,05 mol.
Vì Dung dịch chỉ chứa 2 chất tan ⇒ Cl– đã bị điện phân hết và 2 chất tan đó là Na2SO4 và NaOH.
⇒ mGiảm = mCu + mCl– + mH2
Û mGiảm = 0,05×64 + 0,15×35,5 + 0,05×1 = 8,575 < 10,375
⇒ Nước có điện phân (10,375 – 8,575) = 1,8 gam ⇒ nH2O = 0,1 mol.
⇒ ∑ne nhận = 2nCu + 2nH2 + 2nH2O = 0,1 + 0,05 + 0,2 = 0,35 mol.
⇒ t = ≈ 12602,6s ≈ 3,5 giờ
Đáp án D
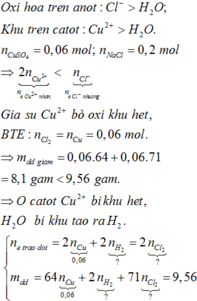
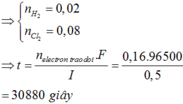
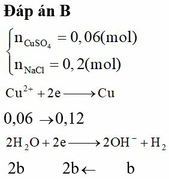
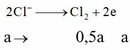
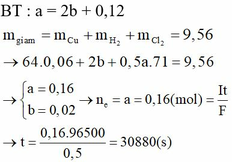

khối lượng dung dịch giảm chính là khối lượng của CuCl2 = x mol và HCl = y mol
Đáp án A