Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
![]()
Thứ tự các phản ứng điện phân xảy ra:

Vì kim loại (gồm Cu và Fe) bị oxi hóa lên số oxi hóa cao nhất nên áp dụng định luật bảo toàn electron ta có:
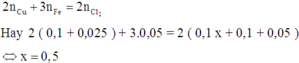

Đáp án B
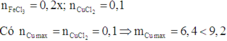
Do đó kim loại thu được gồm Cu và Fe
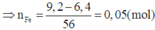
Thứ tự các quá trình nhường và nhận electron ở catot và anot:
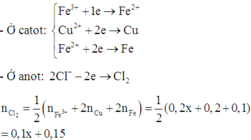
Áp dụng định luật bảo toàn mol electron cho quá trình oxi hóa kim loại (kim loại có số oxi hóa cao nhất), ta có:


Đáp án A
Tại catot có thể lần lượt xảy ra các quá trình:
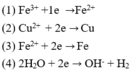
Tại anot có thể lần lượt xảy ra các quá trình:
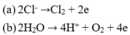
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi thu được hỗn hợp 2 oxit. Trong A có 2 loại ion kim loại
Mặt khác, khi điện phân dung dịch A cho đến khi hết ion Cl - thì catot tăng 6,4 gam
⇒ Quá trình (2) đã xảy ra một phần, Cu 2 + vẫn còn trong dung dịch sau điện phân.
Gọi số mol Fe 3 + , Cu 2 + , Cl - , SO 4 2 - trong 100ml dung dịch A lần lượt là a,b,c,d.
Khi điện phân hết 
Theo bảo toàn e: số e do Fe3+ và Cu2+ nhận bằng số mol Cl- nhường. a + 0,1.2 = c (1)
Khối lượng dung dịch giảm gồm Cu2+ và Cl- đã phản ứng và bị tách ra khỏi dung dịch
6,4 + 35,5c = 17,05 (2)
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi được 16 gam 2 oxit
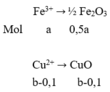
Suy ra: 160,0,5a + 80(b – 0,1) = 16 (3)
Theo định luật bảo toàn điện tích, đối với dung dịch A ta có:
3a + 2b = c + 2d (4)
Giải hệ phương trình ta được:
a = 0,1; b = 0,2; c= 0,3; d = 0,2
Khối lượng muối trong 100ml dung dịch A là 48,25 gam

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
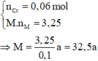
=> a = 2, M = 65 (M là Zn).

Đáp án C
Gọi số mol CuO và MO là a,2a(mol)
TH1:CO khử được MO
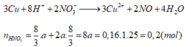
=>a=0,025=>80a+(M+16).2a=4,8=>M là Ca(loại vì CaO không bị CO khử)
Không có M thỏa mãn lọai
TH2.CO không khử đc MO
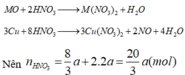
=>a=0,03(mol) =>80a+(M+16).2a=4,8=>M=24
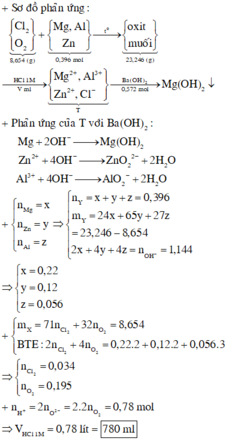

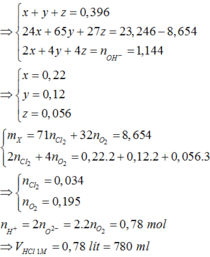

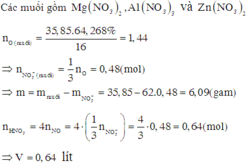
Đáp án C
Vì V lít khí oxi hóa B thành hỗn hợp gồm các oxit và muối clorua nên trong V lít khí này chứa Cl2 và O2.
Sau khi Cl- bị điện phân hết tạo thành Cl2 thì nước mới bị điện phân thay thế ở anot tạo thành O2.
Thứ tự các quá trình nhường – nhận electron xảy ra trong quá trình điện phân:
Do đó Cu2+ chưa bị điện phân hết và Fe2+ chưa bị điện phân
Áp dụng định luật bảo toàn mol electron cho quá trình điện phân, ta có:
Áp dụng định luật bảo toàn mol electron cho quá trình oxi hóa kim loại: