

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



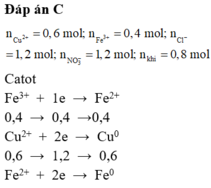


Khi trộn dung dịch ta có phương trình:
3Fe2+ + 4H+ + NO3− → 3Fe3+ + 2H2O + NO
0,2 0,4 1,2 → 0 , 2 3
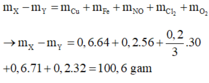

Chọn A.
Tại anot có khí Cl2 và O2 thoát ra với
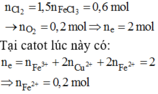
Dung dịch còn lại sau khi lấy catot ra khỏi bình điện phân chứa Fe2+ dư (0,2 mol); H+ (0,8 mol); NO3– (1,2 mol), lúc này tiếp tục xảy ra phản ứng oxi hóa khử nên n H + dư = 0,8 – 4 3 n F e + =8/15 mol
Dung dịch Y chứa Fe3+ (0,2 mol); H+ dư (8/15 mol) và NO3– (1,2 mol). Vậy m X - m Y = 91 , 67

Đáp án : D
nCl- = 0,4 mol => nCl2 = 0,2 mol < n khí anot = 0,4 mol
=> Có điện phân nước ở anot
| Catot Fe3+ + 1e à Fe2+ 0,4 0,4 0,4 Cu2+ + 2e à Cu 0,6 1,2 0,6 2H+ + 2e à H2 0,4 0,4 |
Anot 2Cl- à Cl2 + 2e 1,2 0,6 1,2 2H2O à 4H+ + O2 + 4e 0,8 0,2 0,8 |
=> Còn 0,4 mol Fe2+ ; 0,4 mol H+
3Fe2+ + 4H+ +NO3- è 3Fe3+ + NO + 2H2O
=> nNO = 0,1 mol ( Tính theo H+)
=> mX – mY = mCl2 + mCu + mH2 + mO2 + mNO = 90,8g

Catot: F e 3 + + e → F e 2 +
C u 2 + + 2 e → → C u
F e 2 + + 2 e → F e
· Anot: 2 C l - → C l 2 + 2 e
2 H 2 O → 4 H + + O 2 + 4 e
· nkhí anot = 17 , 92 22 , 4 = 0 , 8 m o l > n C l 2 = 0 , 6 m o l
=> Chứng tỏ ở anot đã xảy ra điện phân H2O.
n o 2 = 0 , 8 - 0 , 6 = 0 , 2 m o l , ne điện phân = 2 . 0 , 6 + 4 . 0 , 2 = 2 mol
· 0,4 + 2.0,6 < 2 < 0,4 + 2.0,6 + 2.0,4
=> Chứng tỏ Fe2+ chưa bị điện phân hết:
n F e đ i ệ n p h â n = 2 - 0 , 4 - 2 . 0 , 6 2 = 0 , 2 mol
· Phản ứng sau điện phân:
3Fe2+ + 4H+ + H N O 3 - → 3Fe3+ + NO + 2H2O
0,2 → 0 , 8 3 0 , 2 3 0,2 0 , 2 3 mol
=> mdư X - mdư Y = m C l 2 + m O 2 + + m C u + m F e + m N O
= 71 . 0 , 6 + 32 . 0 , 2 + 64 . 0 , 6 + 56 . 0 , 2 + 30 . 0 , 2 3 = 100 , 6 g
Gần nhất với giá trị 102.
=> Chọn đáp án B.