Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trộn 50ml dung dịch Ba(OH)2 0,05M với 150ml dung dịch HCl 0,1M thu được 200ml dung dịch A. Tính Cm chất dung dịch A
Giải:
nBa(OH)2 = 1/400 mol
nHCl = 0,015 mol=3/200 mol
ta có pthh:
Ba(OH)2 + 2HCl-------------> BaCl2 + 2H2O
1/400mol 1/200 mol 1/400 mol
Vì 1/200 mol < 3/200 mol nên HCl dư sau pư:
nA = (1/400 + 2/200) mol. = =0,0125 mol
=> CM = A = 0,0125/0,2 = 0,0625 M

Ta có: \(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{HCl}=0,4.1,5=0,6\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{Na_2CO_3}=x\left(mol\right)\\n_{K_2CO_3}=y\left(mol\right)\end{matrix}\right.\)
PT: \(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O+CO_2\)
\(K_2CO_3+2HCl\rightarrow2KCl+H_2O+CO_2\)
\(HCl_{dư}+NaOH\rightarrow NaCl+H_2O\)
Theo PT: \(n_{CO_2}=n_{Na_2CO_3}+n_{K_2CO_3}=x+y\left(mol\right)\) ⇒ x + y = 0,25 (1)
\(n_{HCl\left(pư\right)}=2x+2y\left(mol\right)\) \(\Rightarrow n_{HCl\left(dư\right)}=0,6-2x-2y\left(mol\right)\)
Có: \(\left\{{}\begin{matrix}n_{NaCl}=2n_{Na_2CO_3}+n_{HCl\left(dư\right)}=0,6-2y\left(mol\right)\\n_{KCl}=2n_{K_2CO_3}=2y\left(mol\right)\end{matrix}\right.\)
⇒ 58,5(0,6 - 2y) + 74,5.2y = 39,9 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{0,1.106}{0,1.106+0,15.138}.100\%\approx33,9\%\\\%m_{K_2CO_3}\approx66,1\%\end{matrix}\right.\)
Bạn tham khảo nhé!

nO2=0,085(mol) => nO= 0,17(mol)
m hỗn hợp KL=3,36(g)
nO(trong H2O) = nO(trong O2) = 0,17
=> nH2O = 0,17
=> nH(trong HCl) = nH(trong H2O) = 2nH2O= 0,34
=> nHCl=0,34
=> nCl= 0,34
m muối khan= mKL + mCl = 3,36 + 0,34 x 35,5 = 15,43

Hòa tan 17g hỗn hợp NaOH ,KOH, Ca(OH)2 vào nước được 500g dd X.Để trung hòa 50g dd X cần dung 40g dd HCl 3,65%. Cô cạn dd sau khi trung hòa thu được khối lượng muối khan là?
Các phản ứng xảy ra:
NaOH + HCl → NaCl + H2O
KOH + HCl → KCl + H2O
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Khối lượng hh bazơ tham gia pư: m(hh bazơ) = 17.50/500 = 1,7g
Khối lượng HCl cần dùng: m(HCl) = 40.3,65% = 1,46g
⇒ n(HCl) = 1,46/36,5 = 0,04mol
Số mol H2O tạo thành: n(H2O) = n(HCl) = 0,04mol
Theo ĐL bảo toàn khối lượng:
m(hh bazơ) + m(HCl) = m(muối) + m(H2O) ⇒ m(muối) = m(hh bazơ) + m(HCl) - m(H2O)
⇒ m(muối) = 1,7 + 1,46 - 0,04.18 = 2,44g

Tác dụng với H2SO4 và NaOH
nH2SO4 = 0,0275mol
nNaOH = 0,005mol
=> nH2SO4 phản ứng với Y = 0,025 mol
2R-NH2 + H2SO4 → Muối
0,05 0,025
=> Trong Y có 1 nhóm NH2
Tác dụng với Ba(OH)2
nBa(OH)2 = 0,03 mol
Ta có
=> hh Y gồm R(COOH)(NH2): x mol và R’(COOH)2(NH2): y mol
Ta có x + y = 0,05 và x + 2y = 0,06
=> x = 0,04 và y = 0,01
Đốt cháy Y
nCO2 = 0,13 mol
=> số nguyên tử C trung bình = 2,6
=> Y1: H2N – CH2 – COOH: 0,04 mol
Và Y2: H2N – R’ – (COOH)2: 0,01 (có a nguyên tử C)
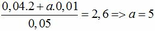
m muối khan = 8,52g = (75 - 1) . 0,01 + (MY2 - 2) . 0,01 + 0,03 . 137 => MY2 = 147
do Y2 có mạch không phân nhánh => Y2 có thể có công thức sau
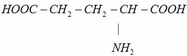
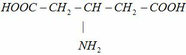

\(m_{ddH_2SO_4}=D\cdot V=1,12\cdot200=224g\)
\(\Rightarrow m_{H_2SO_4}=\dfrac{19,6\%\cdot224}{100\%}=4,3904g\)
\(\Rightarrow n_{H_2SO_4}=0,0448mol\Rightarrow n_{SO_4^{2-}}=n_{H_2SO_4}=0,0488mol\)
\(\Rightarrow m_{SO_4^{2-}}=0,0488\cdot96=4,3008g\)
\(m=m_{SO_4^{2-}}+m_{hhX}=4,3008+6,4=10,7008g\)

Gọi x là nHCl, y là nH2SO4
nNaOH=0.5.0.04=0.02mol
=>nOH-=0.02mol
PT:
H(+)+OH(-)-->H2O
0.02<0.02
=>nH+ trong 10ml hh axit=0.02
=>nH+ trong 100ml hh axit=0.02.10=0.2mol
PT:
H(+)+OH(-)-->H2O
0.2->0.2
=>nNaOH=0.2mol
m muối=mNa(+)+mCl(-)+mSO4(2-)=23.0.2+35.5x...
< = > 35.5x+96y=8.6 (1)
Ta lại có: nH+=x+2y=0.2 (2)
Từ (1)(2)=>x=0.08, y=0.06.
Vậy [HCl]=0.08M, [H2SO4]=0.06M.
Giải rõ nhé!!!!!!!!!
Đặt x, y lần lượt là nồng độ mol/lit của axit H2SO4 và axit HCl
Viết PTHH.
Lập hệ phương trình:
2x + y = 0,02 (I)
142x + 58,5y = 1,32 (II)
Giải phương trình ta được:
Nồng độ của axit HCl là 0,8M và nồng độ của axit H2SO4 là 0,6M.

$n_{HCl} = 0,8.0,5 = 0,4(mol) ; n_{H_2SO_4} = 0,6(mol) ;n_{H_2} = 0,2(mol)$
$n_{H(trong\ axit)} = 0,4 + 0,6.2 = 1,6(mol)$
Bảo toàn H : $n_{H_2O} = \dfrac{n_{H(trong\ axit)} - 2n_{H_2} }{2} = 0,6(mol)$
Bảo toàn khối lượng :
$m = 88,7 + 0,6.18 + 0,2.2 - 0,4.36,5 - 0,6.98 = 26,5(gam)$

xem lại đề có sai không vậy