Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\left\{{}\begin{matrix}nNaCl=x\\nNaBr=y\\nNaI=z\end{matrix}\right.\)
ta có : \(58,5x+103y+150z=5,76\left(1\right)\)
TN1:
\(Br_2+2NaI\rightarrow2NaBr+I_2\)
z ----> z
\(\Rightarrow m_{muối}=mNaBr+mNaCl=103\left(y+z\right)+58,5x=5,29\left(2\right)\)
Từ (1) và (2) => z =0,01
TN2:
\(Cl_2+2NaI\rightarrow2NaCl+I_2\)
0,01 0,01
\(Cl_2+2NaBr\rightarrow2NaCl+I_2\)
\(nNaCl=nCl^-=0,05\rightarrow mNaCl=2,925\left(g\right)\)muối khan ngoài NaCl còn muối khác.Do \(I^-\) có tính khử mạnh hơn \(Br^-\) nên NaI sẽ hết trước và sau hai phản ứng NaBr còn dư.
\(nNaBr\left(dư\right)=t\)
\(\Rightarrow nNaCl=0,05=0,01+y-t+x\)
\(m_{muối}=mNacl+mNaBr\Rightarrow mNaBr_{\left(dư\right)}=3,955-0,05.58,5=1,03\)
\(\Rightarrow t=0,01\)
\(\Rightarrow x+y=0,05\left(3\right)\)
(1) ; (3) ; => \(x=0,02;y=0,03\)
\(\Rightarrow mNaCl=1,17\left(g\right)\)

\(n_{Cl_2}=\dfrac{2,1168}{22,4}=0,0945\left(mol\right)\)
=> nCl(muối) = 0,39 - 0,0945 = 0,201 (mol)
=> nAgCl = 0,201 (mol)
=> mAgCl = 0,201.143,5 = 28,8435 (g)

Quy đổi X thành \(\left\{{}\begin{matrix}FeO:a\left(mol\right)\\Fe_2O_3:b\left(mol\right)\end{matrix}\right.\)
Phần 1: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
=> 127.0,5a + 162,5b = 74,15
=> 63,5a + 162,5b = 74,15 (1)
Phần 2: \(\left\{{}\begin{matrix}FeCl_2:0,5a\left(mol\right)\\FeCl_3:b\left(mol\right)\end{matrix}\right.\)
PTHH: 2FeCl2 + Cl2 --> 2FeCl3
0,5a------------>0,5a
=> 162,5(0,5a + b) = 81,25
=> 0,5a + b = 0,5 (2)
(1)(2) => a = 0,4 (mol); b = 0,3 (mol)
=> m = 0,4.72 + 0,3.160 = 76,8 (g)

Đáp án B
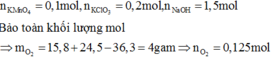
Khi cho hỗn hợp Y phản ứng với HCl đặc sẽ xảy ra phản ứng oxi hóa – khử tạo ra Cl2
![]()
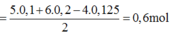


Chọn đáp án C
Gọi số mol của NaBr là x mol; NaI là y mol.
Cho B r 2 vào dung dịch A, chỉ NaI phản ứng.
NaI + 1 2 Br2 → NaBr + 1 2 I2
1 mol NaI → 1 mol NaBr khối lượng giảm 47g
→ n N a I = 7 , 05 47 = 0,15 mol = y
Khi sục khí Clo vào dung dịch A, cả NaBr và NaI phản ứng.
m m u ố i g i ả m = x.(80 – 35,5) + y (127-35,5) = 22,625 g
→ x = 0,2 mol
ð % m N a B r = 0 , 2 . 103 0 , 2 . 103 + 0 , 15 . 150 .100(%) = 47,80(%)

Em có thể tham khảo cách giải sau:
Ta có: mO2 = (15,8 + 24,5)-36,3 = 4 gam. => nO2 = 0,125 mol.
nKMnO4 = 0,1 mol, nKClO3 = 0,2 mol.
Mn7+ + 5e -> Mn2+
Cl5+ + 6e -> Cl-1
2O2- -> O2 + 4e
2Cl-1 -> Cl2 + 2e
Bảo toàn electron, ta có: 0,1*5 + 0,2*6 = 0,125*4 + 2*nCl2
=> nCl2 =0,6 mol.
3Cl2 + 6NaOH -> 5NaCl + NaClO3 + 3H2O (vì đun nóng).
Bđ 0,6 1,5
P/ư 0,6 1,2 1,0 0,2
Sau p/ư 0 0,3 1,0 0,2.
=> m Rắn =0,3*40 + 1,0*58,5 + 0,2*106,5 = 91,8 gam.

Đáp án B
Gọi x, y là số mol NaCl và NaI trong hh X
m(X) = m(NaCl) + m(NaI) = 58,5x + 150y = 104,25g (1)
Sục khí Cl2 dư vào dd A:
NaI + 1/2Cl2 → 1/2I2 + NaCl
y → y
mmuối = m(NaCl) = 58,5.(x+y) = 58,5g
→ x + y = 1mol (2)
Giải hệ PT (1), (2) ta được: x = 0,5mol và y = 0,5mol
mNaCl = 0.5.58,5 = 29,25 (g)

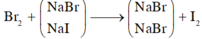
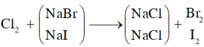
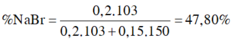
Để thu được NaCl tinh khiết có lẫn NaI người ta dùng Cl2:
Sục khí Cl2 vào dung dịch NaI, khi đó có xảy ra phản ứng:
Ca2 + 2NaI → 2NaCl + I2.
Đun nóng, cô cạn dung dịch thì H2O bay hơi, I2 thăng hoa, ta thu được NaCl tinh khiết.