Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{0,2}=5\)
\(\Rightarrow V_1=5V_2\)
Mà \(V_1+V_2=0,3\)
\(\Rightarrow\left\{{}\begin{matrix}V_1=0,05\left(l\right)\\V_2=0,25\left(l\right)\end{matrix}\right.\)

a) mM (1)= 200*20/100= 40g
mM (2)= 300*5/100=15g
mM= 40+15=55g
mdd= 200+300=500g
C%= 55/500*100%= 11%
b) Đặt: VH2SO4 (1)= x (l)
VH2SO4 (2)= y (l)
nH2SO4 (1)= 1.5x mol
nH2SO4 (2)= 0.3y mol
nH2SO4= 1.5x + 0.3y= 0.3*0.5=0.15 (mol) (1)
VH2SO4= x + y = 0.3 l (2)
Giải (1) và (2):
x= 0.05
y= 0.25
VH2SO4 (1)= 0.05l
VH2SO4 (2)= 0.25l

nH2SO4 cần pha = CM. V = 0,5 . 0,3 = 0,15(mol)
Gọi V1 là thể tích dd H2SO4 1,5M
Gọi V2 là thể tích dd H2SO4 0,5M
Ta có: V1 + V2 = 0,3
1,5V1 + 0,3V2 = 0,15
=> V1 = 0,05
V2 = 0,25

Pha chế dung dịch H 2 S O 4 0,3M.
Gọi x(l) là thể tích của dung dịch axit A.
y(l) là thể tích của dung dịch B.
n H 2 S O 4 ( A ) = C M . V A = 0,2 . x (mol)
n H 2 S O 4 ( B ) = C M . V B = 0,5 . y (mol)
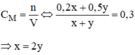
Vậy: ta phải trộn 2 thể tích dung dịch axit A với 1 thể tích dung dịch axit B, ta sẽ được dung dịch H 2 S O 4 có C M = 0,3M.

\(m_{H_2SO_425\%}=\dfrac{150.25}{100}=37,5\left(g\right)\)
Gọi m dd H2SO4 10% là x (g)
Ta có : m dd H2SO4 15% = 150+x (g)
\(m_{H_2SO_415\%}=\dfrac{10x}{100}+37,5=0,1x+37,5\left(g\right)\)
\(15=\dfrac{0,1x+37,5}{x+150}.100\)
\(\rightarrow0,15=\dfrac{0,1x+37,5}{x+150}\)
\(\rightarrow0,05x=15\)
\(\rightarrow x=300\)
Vậy m dd H2SO4 10% là : 300g

Ta có: V A : V B = 2:3
Số mol H 2 S O 4 có trong 2V (l) dung dịch A:
n H 2 S O 4 = C M . V A = 0,2 . 2V = 0,4V (mol)
Số mol H 2 S O 4 có trong 3V (l) dung dịch B:
n H 2 S O 4 = C M . V B = 0,5 . 3V = 1,5V (mol)
Nồng độ mol của dung dịch H 2 S O 4 sau khi pha trộn:
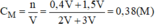
Vậy nồng độ mol của dung dịch C là 0,38M.
Áp dụng sơ đồ đường chéo ta có:
\(\dfrac{V_{H_2SO_4\left(0,3M\right)}}{V_{H_2SO_4\left(1,5M\right)}}=\dfrac{0,5-0,3}{1,5-0,5}=\dfrac{0,2}{1}=0,2\\ \Rightarrow V_{H_2SO_4\left(0,3M\right)}=0,2.V_{H_2SO_4\left(1,5M\right)}\)
Mà \(V_{H_2SO_4\left(0,3M\right)}+V_{H_2SO_4\left(1,5M\right)}=0,3\left(l\right)\)
Thay vào ta được:
\(0,2.V_{H_2SO_4\left(1,5M\right)}+V_{H_2SO_4\left(1,5M\right)}=0,3\\ \Rightarrow V_{H_2SO_4\left(1,5M\right)}=0,1\left(l\right)\\ \Rightarrow V_{H_2SO_4\left(0,3M\right)}=0,2\left(l\right)\)
Vậy.....................
- ta có:
\(\dfrac{V_1}{V_2}\) = \(\dfrac{C_2-C}{C-C_1}\)<=> \(\dfrac{V_1}{0,3-V_1}\)= \(\dfrac{1,5-0,5}{0,5-0,3}\)
=>V1 = 0,25 (l)
=>V2 = 0,3 - 0,25 = 0,05 (l)