Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B.
CO2, SO2 đều là oxit axit nên phản ứng dễ dàng với các dd kiềm, nên có thể dùng Ca(OH)2, NaOH để loại bỏ 2 khí này. Nếu dùng dung dịch KMnO4 hoặc nước Br2 thì không loại bỏ được khí CO2, và còn làm mất C2H4

Đáp án A.
→ n X = 0 , 5 ; n C O 2 = 0 , 15 ; n C O = 0 , 1 → n N 2 = 0 , 25
→
n
X
=
0
,
25
→
n
C
a
C
O
3
=
n
C
O
+
n
C
O
2
=
0
,
125
→
m
=
12
,
5

Đáp án A.
![]()
![]()
→ n X = 0 , 25 → n C a C O 3 = n C O + n C O 2 = 0 , 125 → m = 12 , 5

Tóm tắt:
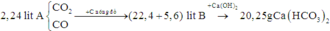
Quan sát – định hướng: Khi cho A qua than nóng đỏ thì chỉ có CO2 tham gia phản ứng tạo CO. Vậy thể tích tăng là do chính phản ứng này tạo ra lượng khí CO nhiều hơn lượng khí CO2 tham gia phản ứng. Đề không cho là phản ứng hoàn toàn và thêm dữ kiện phản ứng với Ca(OH)2.
Chắc chắn trong B còn một lượng khí CO2 chưa phản ứng. Khi cho B qua Ca(OH)2 thì chỉ có CO2 phản ứng được với Ca(OH)2. Qua 2 lần phản ứng đều chỉ có CO2 tham gia phản ứng và qua 2 lần thì CO2 hết.
Từ đó hoàn toàn có thể tính được số mol của CO2.
Ta có phương trình phản ứng:
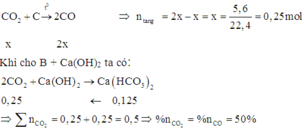
Đáp án D

Đáp án B
C + H 2 O → t 0 C O + H 2 ( 1 ) 0 , 042 → 0 , 042 m o l C + 2 H 2 O → t 0 C O 2 + 2 H 2 ( 2 ) 0 , 014 ← ( 0 , 07 - 0 , 042 ) C O 2 + C a ( O H ) 2 → C a C O 3 + H 2 O ( 3 ) C O + C u O → t 0 C u + C O 2 ( 4 ) 0 , 042 ← ( 0 , 112 - 0 , 07 ) H 2 + C u O → t 0 C u + H 2 O ( 5 ) 0 , 07 0 , 07 ← 0 , 07
Ta có: nCuO= 0,112 mol; n H 2 O = 0,07 mol
Tính toán theo phương trình ta có: 0,042 mol CO; 0,014 mol CO2; 0,07 mol H2
% V C O 2 = % n C O 2 = n C O 2 n X . 100 % = 0 , 014 0 , 014 + 0 , 042 + 0 , 07 . 100 % = 11 , 11 %
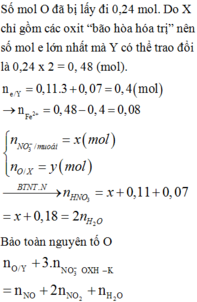
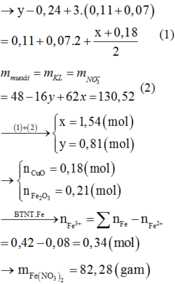
SO2 có S ở trạng thái S+4 có tỉnh khử, dung dịch nước Br2 có tính oxi hóa → SO2 có phản ứng với dung dịch nước Br2. Do vậy khi dẫn hỗn hợp khí đi qua dung dịch nước Br2 thì SO2 bị giữa lại → khí thoát ra là CO2.
Đáp án C