Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng HNO3 nguyên chất là: 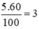 tấn
tấn
Sơ đồ phản ứng điều chế HNO3 từ NH3
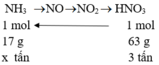
Theo sơ đồ điều chế nHNO3 = nNH3
⇒ mNH3 = 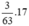 = 0,809524 tấn
= 0,809524 tấn
Khối lượng NH3 hao hụt là 3,8% nghĩa là hiệu suất đạt 100 - 3,8 = 96,2%
Vậy khối lương amoniac cầ dùng là: 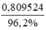 = 0,8415 tấn
= 0,8415 tấn

Đáp án A
Hướng dẫn
Ta có sơ đồ:
(C6H10O5)n → 2nC2H5OH
m(C6H10O5)n = 1000 x 70% = 700 kg.
Theo phương trình:
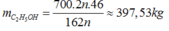
Mà hao hụt 15% → mC2H5OH = 398 x 85% = 337,9 kg

Đáp án: A
Ta có sơ đồ: (C6H10O5)n → 2nC2H5OH
m(C6H10O5)n = 1000 x 70% = 700 kg.
Theo phương trình:
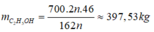
Mà hao hụt 15% → mC2H5OH = 398 x 85% = 337,9 kg

Đáp án A
Hướng dẫn giải:
Ta có sơ đồ: Ca3(PO4)2 → 2P
Ta có: nCa3(PO4)2= 0,5.nP= 0,5.150/31= 75/31 (kmol) → mCa3(PO4)2= (75/31).310= 750 (kg)
→ Khối lượng Ca3(PO4)2 thực tế cần có: 750.100/97=773,2 kg
→Khối lượng quặng photphoric cần lấy là: 773,2.100/65= 1189 kg= 1,189 tấn

N2+ 3H2 ⇌ 2NH3
nNH3= 1mol
Theo phương trình: nN2 (PT)= ½.nNH3= 0,5 mol;
nH2 (PT)= 3/2. nNH3=1,5 mol
Công thức tính hiệu suất:

→nN2(thực tế)=2mol; nH2 (thực tế)= 6 mol
→ VN2(thực tế)=44,8 lít; VH2 (thực tế)= 134,4 lít
Đáp án D

Chọn D
Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
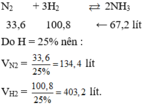
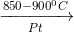 4NO + 6H2O (1)
4NO + 6H2O (1)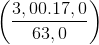 x
x 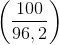 = 0,841 (tấn).
= 0,841 (tấn).
m HNO3 = 5000 . 60% =3000 tấn
HNO3 --- N ----NH3
63g................17g
3000t...........809,5t
m NH3 cần dùng = 809,5 . 100 : (100-3,8) = 841,5 tấn
m HNO3 = 5000 . 60% =3000 tấn
HNO3 --- N ----NH3
63g................17g
3000t...........809,5t
m NH3 cần dùng = 809,5 . 100 : (100-3,8) = 841,5 tấn