Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) nCaCO3 = 0.3 (mol)
CO + O => CO2
=> nO = 0.3 (mol)
mFe = moxit - mO = 16 - 0.3*16 = 11.2 (g)
nFe = 11.2/56 = 0.2 (mol)
nFe : nO = 0.2 : 0.3 = 2 : 3
CT oxit : Fe2O3



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

2yAl +3FexOy -to-> 3xFe + yAl2O3 (1)
phần 1 : Fe +4HNO3 --> Fe(NO3)3 + NO +2H2O (2)
Al2O3 + 6HNO3 --> 2Al(NO3)3 +3H2O (3)
Al +4HNO3 --> Al(NO3)3 +NO +2H2O (4)
P2 : Al2O3 +2NaOH --> 2NaAlO2 +H2O (5)
2Al +2H2O +2NaOH --> 2NaAlO2 +3H2 (6)
vì khi cho phần 2 td vs NaOH dư thấy giải phóng H2 => Al dư sau (1)
nH2=0,015(mol)
nFe(P2)=0,045(mol)
giả sử P1 gấp k lần P2
=> nFe(P1)=0,045k(mol)
theo (5) : nAl(P2)=2/3nH2=0,01(mol)
=>nAl(P1)=0,01k(mol)
nNO=0,165(mol)
theo (2,4) :nNO=(0,045k+0,01k) (mol)
=>0,055k=0,165=> k=3
=>nAl(P1)=0,03(mol)
nFe(p1)=0,135(mol)
\(\Sigma nFe=0,045+0,135=0,18\left(mol\right)\)
\(\Sigma nAl=0,03+0,01=0,04\left(mol\right)\)
mAl2O3=\(14,49-0,135.56-0,03.27=6,12\left(g\right)\)
nAl2O3(P1)=0,06(mol)
=> nAl2O3(P2)=0,02(mol)
\(\Sigma nAl2O3=0,08\left(mol\right)\)
theo (1) : nFe=3x/ynAl2O3
=> 0,18=3x/y.0,08=> x/y=3/4
=>CTHH : Fe3O4
theo (1) :nFe3O4 =1/3nFe=0,06(mol)
=>m=0,04.27+0,06.232=15(g)
bạn Lê Đình Thái ơi bạn giải nhầm tìm m rồi. Cái 0,04 mol đó là mol dư, bạn phải cộng với 0,16 mol phản ứng khi xảy ra phản ứng nhiệt phân nữa.
Kết quả là m=0,2.27+0,06.232=19,32 gam

a)
2Al + 6HCl → 2AlCl3 + 3H2↑
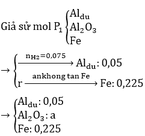
Pt: 2Al + 6H2SO4 → Al2(SO4)3 + 3SO2↑ + 6H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Giả sử P2 = kP1
=> a=0.1
=> m = 128,8g
b)
2yAl + 3FexOy → yAl2O3 + 3xFe
0,1 0,225
=> 0,225y = 0,3x => 3y = 4x
=> Fe3O4

1)Khí sau phản ứng gồm :
CO : a(mol)
CO2:b(mol)
Bảo toàn nguyên tố với C: a + b = \(\dfrac{6,72}{22,4} = 0,3(mol)\)(1)
\(M_{khí} = 20.2 = 40(đvC)\)
Ta có : 28a + 44b = (a + b).40(2)
Từ (1)(2) suy ra : a = 0,075; b = 0,225
\(CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{CO_2} = 0,225(mol)\\ m_{Fe} + m_O = m_{oxit}\\ \Rightarrow n_{Fe} = \dfrac{13,05-0,225.16}{56}=0,16875(mol)\)
Ta thấy : \(\dfrac{n_{Fe}}{n_O} = \dfrac{0,16875}{0,225} = \dfrac{3}{4}\)
Vậy oxit cần tìm : Fe3O4
2) \(\%V_{CO_2} = \dfrac{0,225}{0,225+0,075}.100\% = 75\%\)



a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


Phần 2:
nH2 = 0,03 => nAl dư = 0,02
nNaOH = nAl dư + 2nAl2O3 => nAl2O3 = 0,08
Phần 1:
nAl dư = 0,02k; nAl2O3 = 0,08k; nFe = a
=> 0,02k.27 + 0,08k.102 + 56a = 9.39
nH2 = 0.02k.1,5 + a = 0,105
k = 0.5 và a = 0,09
Fe : O = a : (0,08k.3) => Fe3O4
m2 = 9,39 + 9,39/k =28,17g

Trong hỗn hợp khí, Gọi $n_{CO} = a(mol) ; n_{CO_2} = b(mol)$
Ta có :
$a + b = \dfrac{1,344}{22,4} = 0,06(mol)$
$28a + 44b = (a + b)9.4$
Suy ra a = b = 0,03
$CO + O_{oxit} \to CO_2$
$n_O = n_{CO_2} = 0,03(mol)$
$\Rightarrow n_{Fe} = \dfrac{1,6 - 0,03.16}{56} = 0,02(mol)$
$n_{Fe} : n_O = 0,02 : 0,03 = 2 : 3$
Vậy oxit là $Fe_2O_3$
Khí thu được gồm CO dư và CO2.
PT: \(Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2\)
Ta có: \(n_{CO\left(banđau\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO\left(dư\right)}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\)
⇒ a + b = 0,06 (1)
Mà: Tỉ khối hhk so với He bằng 9
⇒ 28a + 44b = 9.4.0,06 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,03\left(mol\right)\\b=0,03\left(mol\right)\end{matrix}\right.\)
⇒ nCO (pư) = 0,03 (mol)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{y}n_{CO}=\dfrac{0,03}{y}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{1,6}{\dfrac{0,03}{y}}=\dfrac{160}{3}y\left(g/mol\right)\)
\(\Rightarrow56x+16y=\dfrac{160}{3}y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit đó là Fe2O3.
Bạn tham khảo nhé!
a, Số mol các chất: \(nH_2=\dfrac{8,96}{22}.4=0,4\left(mol\right)\)
Số mol \(H_2O=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> Số mol nguyên tử Oxi là 0,4 mol
\(\Rightarrow m_O=0,4.16=6,4\left(g\right)\)
Vậy khối lượng FexOy ban đầu bằng kl hh 2 chất rắn sau phản ứng cộng với kl nguyên tử Oxi mất đi từ
\(Fe_xO_y\): \(m=28.4+6,4=34,8\left(g\right)\)
b, Trong hỗn hợp A kl sắt đôn chất là:
\(m_{Fe}=59,155.28,4=16,8\left(g\right)\Rightarrow n_{Fe}=\dfrac{16,8}{56}=0,3\left(mol\right)\)
Gọi CT của Oxit sắt là \(Fe_xO_y\left(x;y>0\right)\)
Ta có:
\(Fe_xO_y+yH_2\underrightarrow{to}xFe+yH_2O\) (*)
\(.........y.....x.....y\)
\(..0,4mol...0,3mol..0,4mol\)
Theo (*): \(\dfrac{x}{y}=\dfrac{0,3}{0,4}=\dfrac{3}{4}\Rightarrow x=3;y=4\)
Vậy CT của Oxit sắt cần tìm là: \(Fe_3O_4\)